Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. sắt + oxi \(\xrightarrow[]{t^o}\) oxit sắt từ
b. \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
c. Áp dụng định luật bảo toàn khối lượng, ta có:
\(m_{Fe}+m_{O_2}=m_{Fe_3O_4}\)
\(\Rightarrow m_{O_2}=m_{Fe_3O_4}-m_{Fe}=23,3-16,8=6,5\left(g\right)\)
vậy khối lượng khí oxi đã tham gia phản ứng là \(6,5g\)

\(2KClO_3\rightarrow3O_2+2KCl\)
\(m_{KClO_3}=m_{O_2}+m_{KCl}\)
\(\Rightarrow m_{KCl}=m_{KClO_3}-m_{KCl}=24,5-9,6=14,9\left(g\right)\)

a) PTHH: FeCl3 + 3KOH → Fe(OH)3 + 3KCl
b) Theo ĐLBTKL ta có:
\(m_{FeCl_3}+m_{KOH}=m_{Fe\left(OH\right)_3}+m_{KCl}\)
\(\Leftrightarrow m_{FeCl_3}=m_{Fe\left(OH\right)_3}+m_{KCl}-m_{KOH}=2,14+4,47-3,36=3,25\left(g\right)\)

a) $2Al + 3Cl_2 \xrightarrow{t^o} 2AlCl_3$
b) $n_{Al} = \dfrac{5,4}{27} = 0,2(mol)$
Theo PTHH : $n_{Cl_2} = \dfrac{3}{2}n_{Al} = 0,3(mol)$
$\Rightarrow V_{Cl_2} = 0,3.24,79 = 7,437(lít)$
c) $n_{AlCl_3} = n_{Al} = 0,2(mol)$
$\Rightarrow m_{AlCl_3} = 0,2.133,5 = 26,7(gam)$

BT1 :
Bảo toàn khối lượng :
\(m_{FeCl_3}=m_{Fe}+m_{Cl_2}=11.2+21.3=32.5\left(g\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(1.5.....2.25......1.5\)
\(n_{Fe}=\dfrac{9\cdot10^{23}}{6\cdot10^{23}}=1.5\left(mol\right)\)
Số phân tử Cl2 : \(2.25\cdot6\cdot10^{23}=13.5\cdot10^{23}\left(pt\right)\)
Số phân tử FeCl3 : \(1.5\cdot6\cdot10^{23}=9\cdot10^{23}\left(pt\right)\)

a) Fe + 2HCl → FeCl2 + H2 (1)
b) nH2 = 67,2 : 22,4 = 3 mol
Từ pt(1) suy ra : nFe = nH2 = 3 mol
Khối lượng Fe là : mFe = 3 . 56 = 168 g
c) Từ pt(1) => nFeCl2 = nH2 = 3 mol
=> mFeCl2 = 3 . 127 = 381g
a) Fe + 2HCl → FeCl2 + H2
b) \(n_{H_2}=\frac{67,2}{22,4}=3\left(mol\right)\)
Từ PT \(\Rightarrow n_{Fe}=3\left(mol\right);n_{FeCl_2}=3\left(mol\right)\)
\(\Rightarrow m_{Fe}=56.3=168\left(g\right)\)
c) m\(m_{FeCl_2}=3.127=254\left(g\right)\)

a. \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
PTHH : 3Fe + 2O2 -to> Fe3O4
0,3 0,2 0,1
b. \(m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\)
c. \(V_{O_2}=0,2.22,4=4,48\left(l\right)\)
a \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b \(\Rightarrow n_{Fe}=\dfrac{16,8}{56}=0,3mol\) \(\Rightarrow n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=0,1mol\Rightarrow m_{Fe_3O_4}=0,1\cdot232=2,32g\)
c \(\Rightarrow n_{O_2}=\dfrac{2}{3}n_{Fe}=0,2mol\Rightarrow V_{O_2}=0,2\cdot22,4=4,48l\)
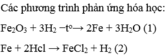
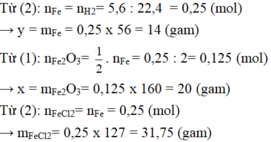
\(a.Sắt+Clo\rightarrow Sắt\left(III\right)clorua\\ b.2Fe+3Cl_2-^{t^o}\rightarrow2FeCl_3\\ c.m_{Fe}+m_{Cl_2}=m_{FeCl_3}\\ \Rightarrow m_{FeCl_3}=5,6+10,65=16,25\left(g\right)\)