Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a) n_{Fe_2O_3} = \dfrac{16.75\%}{160} = 0,075(mol)\\ n_{CuO} = \dfrac{16.25\%}{80} = 0,05(mol)\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{Fe} = 2n_{Fe_2O_3} = 0,15(mol) \Rightarrow m_{Fe} = 0,15.56 = 8,4(gam)\\ n_{Cu} = n_{CuO} = 0,05(mol) \Rightarrow m_{Cu} = 0,05.64 = 3,2(gam)\\ b) n_{H_2} = 3n_{Fe_2O_3} + n_{CuO} = 0,075.3 + 0,05 = 0,275(mol)\\ V_{H_2} = 0,275.22,4 = 6,16(lít)\)

a, mFe2O3 = 32 . 75% = 24 (g)
nFe2O3 = 24/160 = 0,15 (mol)
mCuO = 32 - 24 = 8 (g)
nCuO = 8/80 = 0,1 (mol)
PTHH:
Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
0,15 ---> 0,45 ---> 0,3
CuO + H2 -> (t°) Cu + H2O
0,1 ---> 0,1 ---> 0,1
mFe = 0,3 . 56 = 16,8 (g)
mCu = 64 . 0,1 = 6,4 (g)
b, nH2 = 0,1 + 0,45 = 0,55 (mol)
VH2 = 0,55 . 22,4 = 12,32 (l)
c, PTHH:
2Al + 6HCl -> 2AlCl3 + 3H2
11/30 <--- 1,1 <--- 11/30 <--- 0,55
mAl = 11/30 . 27 = 9,9 (g)
mHCl = 1,1 . 36,5 = 40,15 (g)

mFe2O3=16 . 75%= 12(g) \(\Rightarrow\) n Fe2O3 = \(\frac{12}{160}\) = 0,075 (mol)
mCuO= 4 (g) \(\Rightarrow\) nCuO = 0,05 (mol)
Fe2O3 + 3H2 \(\underrightarrow{t^o}\) 2Fe + 3H2O
0,075 --> 0,225 -->0,15 (mol)
CuO + H2 \(\underrightarrow{t^o}\) Cu + H2O
0,05 --> 0,05 --> 0,05 (mol)
mFe = 0,15 . 56 = 8,4 (g)
mCu = 0,05 . 64= 3,2 (g)
VH2 = (0,225 + 0,05).22,4 = 6,16 (l)

Bài 11:
\(a,n_{Fe_2O_3}=\dfrac{1,6}{160}=0,01\left(mol\right)\\ n_{Cu}=\dfrac{4}{80}=0,05\left(mol\right)\\ PTHH:\\ Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
0,01 -----> 0,03 ---> 0,02
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,05 ---> 0,05 -> 0,05
\(b,m_{Fe}=0,02.56=1,12\left(g\right)\\ m_{Cu}=0,05.64=3,2\left(g\right)\\ V_{H_2}=\left(0,03+0,05\right).22,4=1,792\left(l\right)\)
Bài 12:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ n_{O\left(trong.oxit\right)}=n_{H_2}=0,15\left(mol\right)\\ n_{Fe\left(trong.oxit\right)}=\dfrac{8-0,15,16}{56}=0,1\left(mol\right)\\ CTHH:Fe_xO_y\\ \Rightarrow x:y=0,1:0,15=2:3\\ CTHH:Fe_2O_3\)

hỗn hợp 100% <=> 20g
1. fe2o3 60% <=> 12g <=> 0,075mol
cuo 40% <=> 8g <=> 0,1 mol
Ta có:
Fe2O3 + 3H2 --> 2Fe + 3H2O
mol: 0,075 0,225 0,15
CuO + H2 → Cu + H20
mol: 0.1 0.1 0.1
mFe= 0,15x56=8,4g. mCu=0,1x64= 6,4g
nH2= 0,225+0,1=0,325mol ==> V H2 = 0,325x 22,4 = 7,28 lít

\(n_{Fe_2O_3}=\dfrac{3,2}{160}=0,02mol\)
\(n_{Cu}=\dfrac{8}{80}=0,1mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,02 0,06 0,04 ( mol )
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,1 0,1 0,1 ( mol )
\(m_{Fe}=0,04.56=2,24g\)
\(m_{Cu}=0,1.64=6,4g\)
\(n_{H_2}=0,06+0,1=0,16mol\)
\(n_{Fe_2O_3}=\dfrac{3,2}{160}=0,02mol\)
\(m_{CuO}=\dfrac{8}{80}=0,1mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(CuO+H_2\rightarrow Cu+H_2O\)
\(m_{Fe}=0,02\cdot2\cdot56=2,24g\)
\(m_{Cu}=0,1\cdot64=6,4g\)
\(\Sigma n_{H_2}=0,02\cdot3+0,1=0,16mol\Rightarrow V_{H_2}=3,584l\)
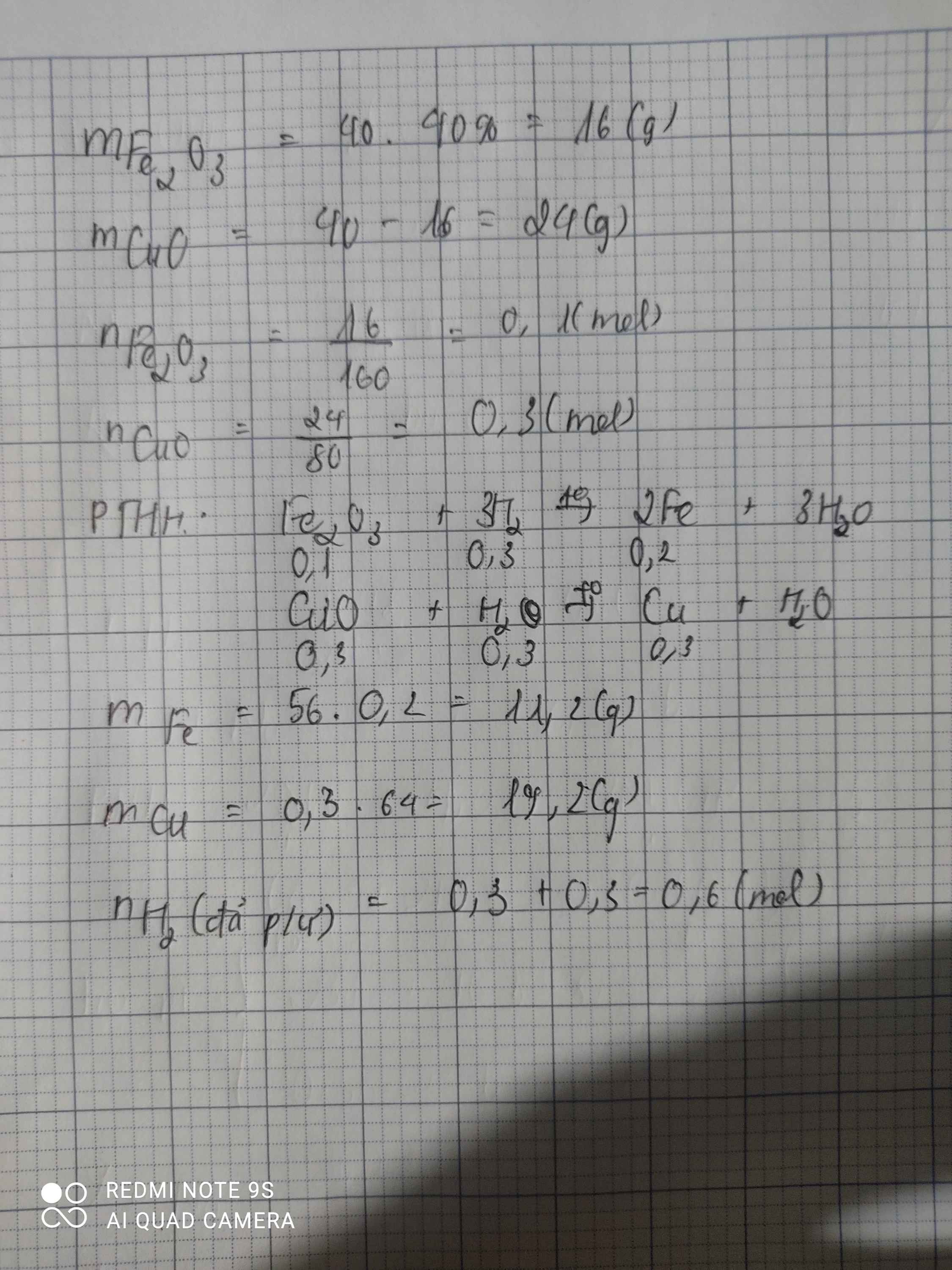

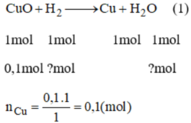
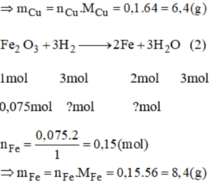
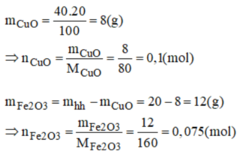

\(m_{Fe_2O_3}=16\cdot75\%=12\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{12}{160}=0.075\left(mol\right)\)
\(n_{CuO}=16\cdot25\%=4\left(g\right)\)
\(n_{CuO}=\dfrac{4}{80}=0.05\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(n_{H_2}=3\cdot0.075+0.05=0.275\left(mol\right)\)
a,\(m_{Fe_2O_3}=16.75\%=12\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
\(m_{CuO}=16-12=4\left(g\right)\Rightarrow n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,075 0,225 0,15
PTHH: CuO + H2 → Cu + H2O
Mol: 0,05 0,05 0,05
\(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right);m_{Cu}=0,05.64=3,2\left(g\right)\)
b,\(n_{H_2}=0,225+0,05=0,275\left(mol\right)\)