Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có: mFe = 40%.m = 0,4m (g) → mCu = m - 0,4m = 0,6m (g)
Sau phản ứng còn 0,65m (g) kim loại > mCu = 0,6m (g)
Khối lượng Fe còn dư: 0,65m - 0,6m = 0,05m (g)
Vậy: mFe phản ứng = 0,4m - 0,05m = 0,35m (g)
Do Fe còn dư sau phản ứng nên tạo thành muối Fe2+
Quá trình nhường electron:
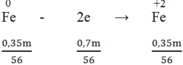
Quá trình nhận electron:
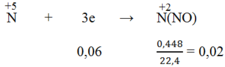
Áp dụng định luật bảo toàn electron, ta có:
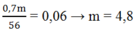
Ta có:
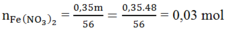
![]()

Đáp án A

Ta có: khối lượng SO2 =m/2.64 = 32m (g)
Khối lượng H2 = n/2.2 = n (g)
Theo đề ra: 32m = 48n
![]()
Vậy M có 2 hóa trị là 2 và 3.
Mặt khác:
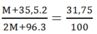
→ M = 56
Vậy M là Fe

Đáp án B.
Khối lượng kim loại phản ứng là 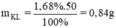
Số mol H2 là 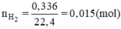
2M + 2n HCl → 2MCl2 + nH2
Số mol của M là:
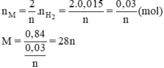
→ {n = 2, M = 56} → M: Fe
Đặt kim loại cần tìm là X, có hóa trị n
Khối lượng kim loại giảm 1,68% → mX phản ứng = 50.1,68% = 0,84 gam
PTHH: 2X+ 2nHCl → 2XCln + nH2
Ta có: nX = (2/n).nH2 ⇔ (0,84/X) = (0,015.2/n)
⇔ X = 28n
Vậy X là Fe
B nha

Đáp án B
Phương trình phản ứng
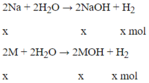
Theo đề bài ta có: 23x +Mx = 6,2 (1)
Áp dụng định luật bảo toàn khối lượng ta có:
mkim loại + mnước = mdd + mhiđro
Từ đó: mhiđro = mkim loại - mnước = mdd = 6,2 + 104 - 110 = 0,2 (g)
⇒x = 0,1 mol, thay vào (1) ta được M = 39 (K)

Đáp án D
Gọi công thức chung của hai muối cacbonat kim loại hóa trị II là RCO3
RCO3 → RO + CO2
Áp dụng định luật bảo toàn khối lượng ta có:
mCO2 = mRCO3 - mRO = 13,4 - 6,8 = 6,6 (g)
⇒ nCO2 = 0,15 mol
Ta có: nNaOH = 0,075 mol
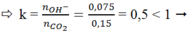
ð tạo ra muối NaHCO3 và CO2 dư.
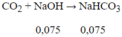
⇒mmuối = 0,075.84 = 6,3(g)

Đáp án B
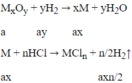
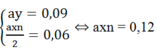
→ ax = 0,12/n
Ta có: (Mx + 16y)a = 4,8
→ Max + 16ay = 4,8 (1)
Thay ay = 0,09 và ax = 0,12/n vào (1)
Ta có: M = 28n → n = 2→ M = 56 : Fe
Thay n = 2 vào ta có: ax = 0,06
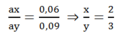
→ Fe2O3
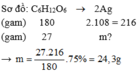

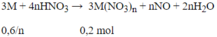
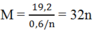
Đáp án B
Khối lượng kim loại phản ứng là:
Số mol H2 là:
2M + 2nHCl → 2MCln + nH2
Số mol của M là:
⇒ M = 28n ⇒ n = 2, M = 56 ⇒ M: Fe