Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Gọi số hạt prroton, nơtron, electron của nguyên tử X là P, N, E và của Y là P’, N’, E’
Theo bài: P = N = E và P’ = N’ = E’
Trong hợp chất XY2, X chiếm 50% về khối lượng nên: ![]() = 1 « P = 2P’
= 1 « P = 2P’
Tổng số proton trong phân tử XY2 là 32 nên P + 2P’ = 32
Từ đây tìm được: P = 16 (S) và P’ = 8 (O)
Hợp chất cần tìm là SO2
Cấu hình electron của S: 1s22s22p63s23p4 và của O: 1s22s22p4

Đáp án A.
Gọi số hạt proton, nơtron, electron của nguyên tử X là p, n, e và của Y là p’, n’, e’.
Theo bài : p = n = e và p’ = n’ = e’.
Trong hợp chất XY2, X chiếm 50% về khối lượng nên:
![]()
Tổng số proton trong phân tử XY2 là 32 nên p + 2p’ = 32.
Từ đây tìm được: p = 16 (S) và p’ = 8 (O). Hợp chất cần tìm là SO2.
Cấu hình electron của S: 1s22s22p63s23p4 và của O: 1s22s22p4.

Chọn A
Y chiếm 50% về khối lượng → MX = 2MY → nX + pX = 2 nY + 2 pY (1)
nX = pX; nY = pY (2)
pX + 2pY = 32 (3)
→ pX = 16 (S): [Ne]3s23p4; pY = 8 (O): [He]2s22p4
Liên kết trong phân tử SO2 là liên kết cộng hóa trị.

Đáp án C
Tổng số proton trong MX2 là 58 hạt
→ ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt
→ -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX
= (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng
![]()
![]()
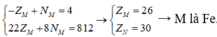
![]()
Cấu hình electron của M là [Ar]3d64s2.

Chọn C
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số nơtron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số nơtron bằng số proton → ZX = NX
MH =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX = 58 + NM + 58 - ZM = 116 + NM - ZM


Nếu X(Z=16) thì cấu hình e là 1s2 2s2 2p6 3s2 3p4
Y (Z=8) cấu hình e là 1s2 2s2 2p4
Đúng không ạ ?
Trong phân tử XY2, X chiếm 50% về khối lượng
=> \\(\\dfrac{A_X}{A_X+2A_Y}=\\dfrac{1}{2}\\Rightarrow A_X=2A_Y\\)
Vì trong hạt nhân của X bà Y đều có số p=n
=> AX = AY <=> NX + PX = 2(NY+PY) <=> PX+PX = 2(PY+PY)
<=> PX =2PY
Vì tổng số proton trong XY2 bằng 32
=> PX = 16; PY=8
X(Z=16) có cấu hình e là 1s2 2s22p6 3s23p4.
=> X nằm ở ô số 16, chu kì 3, nhóm VIA.
Y(Z=8) có cấu hình e là 1s2 2s22p4.
=> Y nằm ở ô số 8, chu kì 2, nhóm VIA.
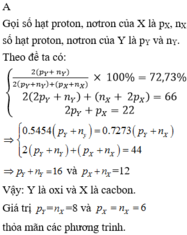


Đáp án A.
Gọi số hạt proton, nơtron, electron của nguyên tử X là p, n, e và của Y là p’, n’, e’.
Theo bài : p = n = e và p’ = n’ = e’.
Trong hợp chất XY2, X chiếm 50% về khối lượng nên:
M X 2 M Y = 50 50 ⇒ p + n 2 ( p ' + n ' ) = 1 ⇒ p = 2 p '
Tổng số proton trong phân tử XY2 là 32 nên p + 2p’ = 32.
Từ đây tìm được: p = 16 (S) và p’ = 8 (O). Hợp chất cần tìm là SO2.
Cấu hình electron của S: 1s22s22p63s23p4