Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

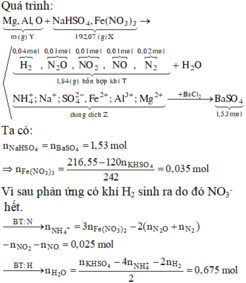
n(KHSO4) = n(BaSO4) = 1,53 mol ⇒ n(Fe(NO3)3) = 0,035 mol
nT = 0,09 mol
Ta thấy 2 khí còn lại là NO và N2 với số mol lần lượt là x; y
Từ n(H2) : n(N2O) : n(NO2) = 4/9 : 1/9 : 1/9
⇒n(H2) = 0,04 mol; n(N2O) = 0,01 mol; n(NO2) = 0,01 mol
⇒mT = 30x + 28y + 0,04×2 + 0,01×44 + 0,01×46 = 1,84 g
Lại có: x + y = 0,09 − 0,04 − 0,01 − 0,01 = 0,03 mol
⇒ x = 0,01; y = 0,02 mol
Bảo toàn N: Giả sử trong muối có NH4+
n(NH4+) = 3n(Fe(NO3)3) – nN(T) = 0,025 mol
Bảo toàn H:
n(H2O) = 1/2n(KHSO4) − 2n(H2) − 4n(NH4+) = 0,675 mol
Bảo toàn O:
4n(KHSO4) + 9n(Fe(NO3)3) + nO(Y) = nH2O + nO(T) + 4nSO4
⇒ nO(Y) = 0,4 mol ⇒ mY = 0,4×16:64/205 = 20,5 g
→ Đáp án B

Đáp án : B
, nKHSO4 = nBaSO4 = 1,53 mol à nFe(NO3)3 = 0,035 mol
, nD = 0,09 mol . Ta thấy 2 khí còn lại là NO và N2 với số mol lần lượt là x;y
Từ nH2 : nN2O : nNO2 = 4/9 : 1/9 : 1/9
=> nH2 = 0,04 mol ; nN2O = 0,01 ; nNO2 = 0,01 mol
=> mD = 30x + 28y + 0,04.2 + 0,01.44 + 0,01.46 = 1,84g
Lại có : x + y = 0,09 – 0,04 – 0,01 – 0,01 = 0,03 mol
=> x = 0,01 ; y = 0,02 mol
Bảo toàn N : Giả sử trong muối có NH4+ => nNH4+ = 3nFe(NO3)3 – nN(D) = 0,025 mol
Bảo toàn H : nH2O = ½ (nKHSO4 – 2nH2 – 4nNH4+ ) = 0,675 mol
Bảo toàn O : 4nKHSO4 + 9nFe(NO3)3 + nO(B) = nH2O + nO(D) + 4nSO4
=> nO(B) = 0,4 mol => mB = 0,4.16 : (64/205) = 20,5g

Đáp án : C
nKHSO4 = nBaSO4 = 1,53 mol ® nFe(NO3)3 = 0,035 mol
, nT = 0,09 mol . Ta thấy 2 khí còn lại là NO và N2 với số mol lần lượt là x;y
Từ nH2 : nN2O : nNO2 = 4/9 : 1/9 : 1/9
=> nH2 = 0,04 mol ; nN2O = 0,01 ; nNO2 = 0,01 mol
=> mT = 30x + 28y + 0,04.2 + 0,01.44 + 0,01.46 = 1,84g
Lại có : x + y = 0,09 – 0,04 – 0,01 – 0,01 = 0,03 mol
=> x = 0,01 ; y = 0,02 mol
Bảo toàn N : Giả sử trong muối có NH4+ => nNH4+ = 3nFe(NO3)3 – nN(T) = 0,025 mol
Bảo toàn H : nH2O = ½ (nKHSO4 – 2nH2 – 4nNH4+ ) = 0,675 mol
Bảo toàn O : 4nKHSO4 + 9nFe(NO3)3 + nO(Y) = nH2O + nO(T) + 4nSO4
=> nO(Y) = 0,4 mol => mY = 0,4.16 : (64/205) = 20,5g

Chọn D
Đáp án A sai, vì lượng Fe tạo thành nếu cho tiếp H 2 S O 4 dư vào thì Fe bị hòa tan hết.
Đáp án B sai, vì C u S O 4 sẽ phản ứng hết với Mg và Fe dẫn đến chỉ thu được kim loại Cu.
Đáp án c sai, vì A g N O 3 sẽ phản ứng hết với Mg và Fe dẫn đến chỉ thu được Ag và AgI.
Đáp án D đúng, vì khi Z n 2 + dư loại hết Mg ra thì Zn tiếp tục bị hòa tan bới NaOH thu được Fe
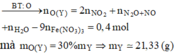
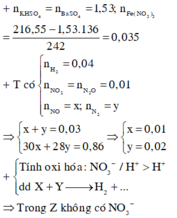

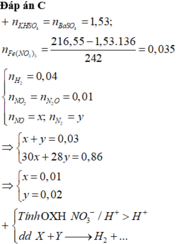
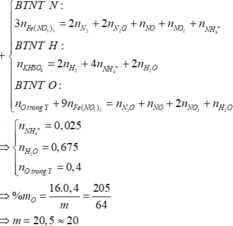



Đáp án : D
Giả sử có 1 mol hỗn hợp gồm x mol Al2(SO4)3 và (1 – x) mol K2SO4
=> tổng số mol các nguyên tố
= nAl + nK + nS + nO = 2x + 2.(1 – x) + (3x + 1 – x) + 4.( 3x + 1 – x) = 10x + 7
=>nO = nngto.%nO
=> 4.(3x + 1 – x) = (10x + 7).20/31
=> x = 1/3 mol
=> mhh đầu = 230g
Khi phản ứng với BaCl2 thì nBaSO4 = nSO4 = 3x + 1 – x = 5/3 mol
=> mBaSO4 = 388,3g
=> mBaSO4 : mhh = 1,688 lần