Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Áp dụng phương trình Cla-pe-ron-Men-de-le-ep cho hai lượng khí ở ngăn trên và dưới ta có
\(P_1 V_1 = n_1 RT_1(1)\)
\(P_2 V_2 = n_2 RT_2(2)\)
chia hai vế của phương trình ta được
\(\frac{P_1V_1}{P_2V_2} = \frac{n_1}{n_2}\frac{T_1}{T_2} \)
\(P_2 = 2P_1; T_1 = 400K, V_1 = V_2, n_2 = 3n_1\)
=> \(\frac{1}{2} = \frac{1}{3}\frac{T_1}{T_2}\)
=> \(T_2 = \frac{2}{3}T_1 = 266,67K.\)
Một bình hình trụ cao l0 = 20cm chứa không khí ở 37oC. Người ta lộn ngược bình và nhúng vào chất lỏng có khối lượng riêng d = 800kg/m3 cho đáy ngang với mặt thoáng chất lỏng. Không khí bị nén chiếm 1/2 bình.
a. Nâng bình cao thêm một khoảng l1 = 12cm thì mực chất lỏng trong bình chênh lệch bao nhiêu so với mặt thoáng ở ngoài ?
b. Bình ở vị trí như câu a. Nhiệt độ của không khí bằng bao nhiêu thì không có chênh lệch nói trên nữa ? (áp suất khí quyển Po = 9,4.104 Pa lấy g = 10m/s2)
làm hộ mình bài này với

Khi khóa K mở (bình đã thông nhau). Gọi p 1 ' và p 2 ' là áp suất riêng phần của chất khí thứ nhất và thứ hai.
Khi đó áp suất của hỗn hợp khí trong bình là:
p = p 1 ' + p 2 ' (1)
Xét chất khí trong bình A và B khi khóa K đóng và mở.
Theo định luật Bôi-lơ – Ma-ri-ốt ta có:
p 1 V 1 = p 1 ' ( V 1 + V 2 )
⇒ p 1 ' = p 1 V 1 V 1 + V 2 (2)
p 2 V 2 = p 2 ' ( V 1 + V 2 )
⇒ p 2 ' = p 2 V 2 V 1 + V 2 (3)
Thay (2) và (3) vào (1) ta được:
p = p 1 ' + p 2 ' = p 1 V 1 + p 2 V 2 V 1 + V 2
= 1 , 6.3 + 3 , 4.4 , 5 3 + 4 , 5 = 2 , 68 a t

Đáp án: D
Khi không dãn nở, lực nâng pit-tong một đoạn h là:
A = F.h = pS.h = p(V – V0).
Qua trình đẳng áp:
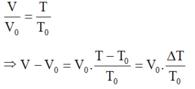
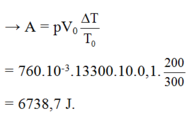
Khi 1,5 g xăng cháy hết sẽ tỏa ra nhiệt lượng:
Q = m.q = 1,5.10-3.4.107J = 60000J.
Vậy H = A/Q = 0,11 = 11%.

Đáp án D
Tới nhiệt độ nào thì van mở:
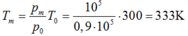
Bắt đầu từ nhiệt độ T m áp suất trong bình 1 tăng nhanh hơn trong bình 2,
nhưng khi hiệu áp suất vượt quá 105Pa thì van lại mở. Van giữ cho hiệu áp suất là 105Pa trong quá trình tăng nhiệt độ cho đến khi T = 500K. Khi đó:
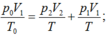
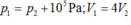
Ta có ![]() , từ đó rút ra
, từ đó rút ra ![]()

Đáp án: C
Ta có:
- Trạng thái 1: T 1 = 27 + 273 = 300 K V 1 = l 1 S
- Trạng thái 2: T 2 = 27 + 10 + 273 = 310 K V 2 = l 2 S
Áp dụng định luật Gay Luy-xác, ta có:
V 1 T 1 = V 2 T 2 ↔ l 1 S T 1 = l 2 S T 2
→ l 2 = l 1 T 2 T 1 = 20.310 300 = 20,67 c m

Gọi ρ 1 và ρ 2 là khối lượng riêng của không khí ở nhiệt độ T 1 = 27 + 273 = 300 K và nhiệt độ T 2 là nhiệt độ khi khí cầu bắt đầu bay lên.
Khi khí cầu bay lên:
F Á c - s i - m é t = P v ỏ k h í c ầ u + P c ủ a k h ô n g k h í n ó n g
ρ 1 gV = mg + ρ 2 gV
ρ 2 = ρ 1 – m/V (1)
Ở điều kiện chuẩn, khối lượng riêng của không khí là:
ρ 0 = 29g/22,4l = 1,295g/ d m 3 = 1,295kg/ m 3
Vì thể tích của một lượng khí tỉ lệ thuận với nhiệt độ tuyệt đối khi áp suất không đổi nên khối lượng riêng của một lượng khí tỉ lệ nghịch với nhiệt độ tuyệt đối khi áp suất không đổi.
Ta có: ρ 1 = T 0 ρ 0 / T 1 (2)
Từ (1) và (2) suy ra: ρ 1 = 1,178 kg/ m 3
Do đó ρ 2 = 0,928 kg/ m 3
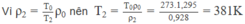
t 2 = 108 ° C

Trạng thái ban đầu: \(\left\{{}\begin{matrix}p_1=3atm\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái sau: \(\left\{{}\begin{matrix}p_2=???\\T_2=127^oC=400K\end{matrix}\right.\)
Áp dụng quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{3}{300}=\dfrac{p_2}{400}\Rightarrow p_2=4atm\)

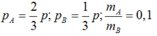
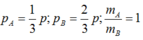
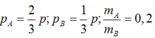

Đáp án B
Gọi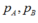 là áp suất riêng phần ban đầu của từng chất khí, ta có :
là áp suất riêng phần ban đầu của từng chất khí, ta có :
a) từ đó rút ra :
b) Tỉ số mol của hai chất bằng tỉ số áp suất riêng phần ban đầu :
Từ đó rút ra :
Ap dụng hằng số :