Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn B
![]()
Gọi số mol của CaC O 3 và MgC O 3 lần lượt là x và y mol

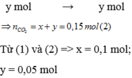
![]()
![]()

\(n_{CaCO_3}=a\left(mol\right),n_{MgCO_3}=b\left(mol\right)\)
\(m=100a+84b=14.2\left(g\right)\left(1\right)\)
\(n_{CO_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(CaCO_3\underrightarrow{^{^{t^0}}}CaO+CO_2\)
\(MgCO_3\underrightarrow{^{^{t^0}}}MgO+CO_2\)
\(\Rightarrow a+b=0.15\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.05\)
\(\%CaCO_3=\dfrac{0.1\cdot100}{14.2}\cdot100\%=70.42\%\)
\(\%MgCO_3=29.58\%\)

Gọi số mol MgCO3, CaCO3 là a, b (mol)
=> 84a + 100b = 1,84 (1)
PTHH: MgCO3 --to--> MgO + CO2
a-------------------->a
CaCO3 --to--> CaO + CO2
b-------------------->b
=> a + b = \(\dfrac{0,448}{22,4}=0,02\) (2)
(1)(2) => a = 0,01 (mol); b = 0,01 (mol)
=> \(\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{0,01.84}{1,84}.100\%=45,65\%\\\%m_{CaCO_3}=\dfrac{0,01.100}{1,84}.100\%=54,35\%\end{matrix}\right.\)

Câu 1:
PTHH: \(CaCO_3\underrightarrow{to}CaO+CO_2\\ xmol:xmol\rightarrow xmol\)
\(MgCO_3\underrightarrow{to}MgO+CO_2\\ymol:ymol\rightarrow ymol\)
Gọi x và y lần lượt là số mol của \(CaCO_3\) và \(MgCO_3\)
\(m_{hh}=m_{CaCO_3}+m_{MgCO_3}\)
\(\Leftrightarrow100x+84y=14,2\left(g\right)\left(1\right)\)
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Leftrightarrow x+y=0,15\left(mol\right)\left(2\right)\)
Giải phương trình (1) và (2) ta được: \(\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m_{CaCO_3}=100.0,1=10\left(g\right)\\m_{MgCO_3}=14,2-10=4,2\left(g\right)\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}\%m_{CaCO_3}=\dfrac{10}{14,2}.100\%=70,4\%\\\%m_{MgCO_3}=100\%-70,4\%=29,6\%\end{matrix}\right.\)
câu 2 :
nCaCO3 = \(\dfrac{40}{100}\) = 0,4 mol
nCO2 = \(\dfrac{5,6}{22,4}\) = 0,25 mol
CaCO3 \(^{to}\rightarrow\)CaO + CO2 \(\uparrow\)
0,25 \(\leftarrow\)0,25
- các chất sau phản ứng : CaO ; CaCO3 dư
mCaO = 0,25 . 56 = 14 g
mCaCO3 = (0,4 - 0,25 ) . 100 = 15 g

MgCO3 ----> MgO + CO2
CaCO3 -----> CaO + CO2
0,15 (mol) <------------ 0,15 (mol) (1) đây ý nói là tổng lượng mol CO2 = tổng lượng hỗn hợp muối
MgCO3 + HCl -------> MgCl2 + CO2 + H20
CaCO3 + HCl --------> CaCl2 + CO2 + H20
=> n(MgCO3,CaCO3) = n(MgCl2,CaCl2) = 0,15 (mol)
=> M(MgCl2,CaCl2) = 317/3
Sau đó, ta đặt: C (là phần trăm của CaCl2 trong hỗn hợp muối)
1-C (là phần trăm của MgCl2 trong hỗn hợp muối)
Với C là 100% trong hỗn hợp đó
=> 111C + 95x(1-C) = 317/3
Từ đó suy ra: C= 2/3
Vì lượng muối trong hỗn hợp tác dụng với HCl bằng lượng từng muối trong hỗn hợp ban đầu nên
%CaCO3 = 2/3x100% = 66,667%
%MgCO3 = 1/3x100% = 33,33%

Áp dụng định luật BTKL :
\(m_{CO_2}=142-76=66\left(g\right)\)
\(n_{CO_2}=\dfrac{66}{44}=1.5\left(mol\right)\)
\(V_{CO_2}=1.5\cdot22.4=33.6\left(l\right)\)
\(n_{CaCO_3}=a\left(mol\right),n_{MgCO_3}=b\left(mol\right)\)
\(m_X=100a+84b=142\left(g\right)\left(1\right)\)
\(CaCO_3\underrightarrow{^{^{t^0}}}CaO+CO_2\)
\(MgCO_3\underrightarrow{^{^{t^0}}}MgO+CO_2\)
\(m_Y=56a+40b=76\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=1,b=0.5\)
\(\%CaO=\dfrac{56\cdot1}{76}\cdot100\%=73.68\%\)
\(\%MgO=100-73.68=26.32\%\)
PTHH: \(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\uparrow\)
a_______a_____a (mol)
\(MgCO_3\xrightarrow[]{t^o}MgO+CO_2\uparrow\)
b_______b_____b (mol)
Ta lập hệ phương trình: \(\left\{{}\begin{matrix}100a+84b=142\\56a+40b=76\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=1\\b=0,5\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CaO}=\dfrac{56}{76}\cdot100\%\approx73,68\%\\\%m_{MgO}=26,32\%\\V_{CO_2}=\left(1+0,5\right)\cdot22,4=33,6\left(l\right)\end{matrix}\right.\)

CaCO3 + H2SO4 --> CaSO4 + CO2 + H2O
x x x
MgCO3 + H2SO4 --> MgSO4 + CO2 + H2O
y y y
nCO2=\(\dfrac{0,896}{22,4}\)=0,04
100x+84y=3,68
x+y=0,04
\(\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
%mCaCO3=\(\dfrac{0,02.100}{3,68}\)=54,35%
%mMgCO3=100-54,35=45,65%
mCaSO4=0,02.136=2,72g
mMgSO4=0,02.120=2,4g

MgCO3 ----> MgO + CO2
CaCO3 -----> CaO + CO2
0,15 (mol) <------------ 0,15 (mol) (1) đây ý nói là tổng lượng mol CO2 = tổng lượng hỗn hợp muối
MgCO3 + HCl -------> MgCl2 + CO2 + H20
CaCO3 + HCl --------> CaCl2 + CO2 + H20
=> n(MgCO3,CaCO3) = n(MgCl2,CaCl2) = 0,15 (mol)
=> M(MgCl2,CaCl2) = 317/3
Sau đó, ta đặt: C (là phần trăm của CaCl2 trong hỗn hợp muối)
1-C (là phần trăm của MgCl2 trong hỗn hợp muối)
Với C là 100% trong hỗn hợp đó
=> 111C + 95x(1-C) = 317/3
Từ đó suy ra: C= 2/3
Vì lượng muối trong hỗn hợp tác dụng với HCl bằng lượng từng muối trong hỗn hợp ban đầu nên
%CaCO3 = 2/3x100% = 66,667%
%MgCO3 = 1/3x100% = 33,33%

a. Các phương trình có thể xảy ra:
C + O2 → t ∘ CO2 (1)
CaCO3 → t ∘ CaO + CO2 (2)
MgCO3 → t ∘ MgO + CO2 (3)
CuCO3 → t ∘ CuO + CO2 (4)
C +CO2 → t ∘ 2CO (5)
C + 2CuO → t ∘ 2Cu + CO2 (6)
CO + CuO → t ∘ Cu + CO2 (7)
CaO + 2HCl →CaCl2 + H2O (8)
MgO + 2HCl →MgCl2 + H2O (9)
CuO + 2HCl →CuCl2 + H2O (10)
b. Vì sau phản ứng có CO và CO2, các phản ứng xảy ra hoàn toàn nên các chất còn lại sau khi nung là CaO, MgO và Cu không có phản ứng (10)
mCu = 3,2(g) => mCuCO3 = 6,2g
Gọi số mol CaCO3, MgCO3, C trong hỗn hợp lần lượt là a, b, c.(*)
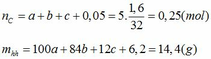
Giải ( *), (**), (***) ta được a=0,025; b=0,05; c=0,125.