Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tổng số hạt trong phân tử Y là 214 hạt.
4(2pM + nM) + 3(2pX + nX) = 214 (1)
Ion M3+ có số electron bằng số electron của ion X4−
pM - 3 = pX + 4 => pX = pM - 7 (2)
Tổng số hạt proton, nơtron, electron của nguyên tử nguyên tố M nhiều hơn tổng số hạt của nguyên tử nguyên tố X trong Y là 106
4(2pM + nM) - 3(2pX + nX) = 106 (3)
(1), (3) => 2pM + nM = 40 (4) và 2pX + nX = 18 (5)
(2), (4), (5) => pX = 6 ; pM = 13 => X là C, M là Al.
=> Y là Al4C3
Cre : khoahoc.vietjack.com

Theo đề bài ta có :
4pM + 2nM + 2pX + nX = 140 (1)
4pM + 2pX = 44 + 2nM + nX (2)
pM + nM = pX + nX + 23 (3)
4pM + 2nM = 4pX + 2nX + 62 (4) ( nhân 2 vế với 2)
Ta có :
Từ (1) và (4)
=> 6pX + 3nX = 78
Từ (1) và (2)
=> 4nM + 2nX = 96
Từ (3) và (4)
=> pM = pX + 8
Từ (1)
=> 4pM + 2nM + 2pX + nX = 140
=> 4pX + 32 + 2nM + 2pX + nX = 140
=> 6pX +2nM + nX = 108
=> 12pX + 4nM + 2nX = 216
Lại có : 4nM + 2nX = 96 (từ 1 và 2)
=> 12pX = 216 - 96 = 120
=> pX = 10
=> pM = 10 + 8 = 18
Từ (1) và (4)
=> 6pX + 3nX = 78
=> 60 + 3nX = 78
=> nX = 6
=> MX = 6 + 10 = 16 (Oxi)
Từ (1) và (2)
=> 4nM + 2nX = 96
=> nM = 21
=> MM = 21 + 18 = 39 (kali)
=> CTHH : K2O
Câu 1
Trong phân tử M2X có
2( 2p1 + n1 ) + 2p2 + n2 = 140 (1)
4p1 + 2p2 = 2n1 + n2 + 44 (2)
Theo đề bài.
p1 + n1 = p2 + n2 + 23 (3)
2p1 + n1 - 1 = 2p2 + n2 + 2 + 31 (4)
Giải hệ gồm (1) và (2) ta có
4p1 + 2p1 = 92
Trừ (3) cho (4) ta được
- p1 + 1 = - p2 - 10
<=> p1 - p2 = 11
Kết hợp lại có hệ sau
4p1 + 2p1 = 92
p1 - p2 = 11
Giải hệ tìm được p1 = 19 và p2 = 8
=> M là Kali và X là Oxi
Cấu hình:
K19 1s^2 2s^2 2p^6 3s^2 3p^6 4s^1
O8 1s^2 2s^2 2p^4

1
Ta có hệ: SM + SX = 84 và SM - SX = 36
\(\rightarrow\) Giải hệ được SM = 60; SX= 24.
ZM ≤ 60:3=20 \(\rightarrow\) Ca, ZX ≤ 24 :3=8 \(\rightarrow\)O Vậy MX là CaO
2
Giải theo S ta có: SM + 2Sx= 186
Tổng số hạt trong M2+ là SM - 2 ( Vì mất 2e), còn X là Sx + 1 ( Vì nhận thêm 1e)
Vậy có phương trình 2 là SM - 2 - (Sx + 1) =27
Giải hệ ta được SM = 82 \(\rightarrow\) ZM= 26; với Sx =52 \(\rightarrow\)Zx = 17 Vậy MX2 là FeCl2
1: có hơp chất A là MX
có 2pM+nM+2pX+nX=84(1)
2pM-nM+2pX-nX=28(2)
2pM+2-2pX+2=20(3)
lấy (1)+(2)<=> 4pM+4pX=112(4)
giai ge (3) và (4)
pM=20
pX=8
chất là CaO
2: gọi zM là số proton của M, nM là số nơ-tron của M, zX là số proton của X, nX là số nơ-tron của X
Tổng số proton trong hợp chất là Z (với Z=zM+zX), tổng số nơ-tron là N (với N=nM+nX)
số khối của ion M2+ là aM (bằng zM+nM), của ion X- là aX (bằng zX+nX) ==> có điều này vì trong ion chỉ có số electron thay đổi, số proton và nơ-trơn KHÔNG đổi
tổng số hạt của ion M2+ là bằng zM+(eM-2)+nM (ion 2+ thiếu 2 electron) = 2zM+nM-2
tổng số hạt của ion X- là bằng zX+(eX+1)+nX (ion 1- dư 1 electron) = 2zX+nX+1
---
phân tử MX2 có tổng số hạt 186 --> 2zM+nM+2zX+nX=186 --> 2Z+N=186 (1)
số hạt mang điện nhiều hơn số hạt không mang điện là 54
--> 2zM+2zX-(nM+nX)=54 --> 2Z-N=54 (2)
(1),(2) --> Z=60, N=66
số khối của ion M2+ nhiều hơn số khối của ion X- là 21
--> aM-aX=21
--> (zM-zX)+(nM-nX)=21 (3)
tổng số hạt của ion M2+ nhiều hơn tổng số hạt của ion X- là 27
--> 2zM+nM-2-2zX-nX-1=27
---> 2(zM-zX)+(nM-nX)=30 (4)
Đặt zM-zX=S, nM-nX=T, ta có hệ phương trình theo S và T
--> S=9, T=12
--> zM-zX=9 (5)
Z=60 --> zM+zX=60 (6)
(5), (6) --> zM=26, zX=17
--> M là Fe
--> X là Cl

3/ nhỗn hợp = 8,4.1023 : 6.1023 = 1,4 (mol)
nO = 230,4 : 16 = 14,4 (mol)
Gọi nCa3(PO4)2 = x (mol) \(\rightarrow\) nO = 8x (mol)
\(\rightarrow\) nAl2(SO4)3 = 1,4-x (mol) \(\rightarrow\) nO = 12.(1,4-x) (mol)
\(\rightarrow\) 8x + 12.(1,4-x) = 14,4 \(\rightarrow\) x = 0,6 (mol)
nCa3(PO4)2= 0,6 (mol) \(\rightarrow Ca_3\left(PO_4\right)_2=\) 0,6.310 = 186 (g)
nAl2(SO4)3= 1,4-x = 0,8 (mol) \(\rightarrow^mAl_2\left(SO_4\right)_3\) = 0,8 . 342 = 273,6 (g)

1) Nguyên tử X có tổng số hạt là 18.Tìm tên nguyên tố X.
Gọi p, e, n là........ của X
Ta có: \(2p+n=18\)
\(\Rightarrow n=18-2p\) \(\left(I\right)\)
Mặt khác: \(p\le n\le1,5p\)
\(\Leftrightarrow p\le18-2p\le1,5p\)
\(\Rightarrow\left\{{}\begin{matrix}p\le18-2p\\18-2p\le1,5p\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}3p\le18\\3,5p\ge18\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}p\le6\\p\ge5,1\end{matrix}\right.\)
\(\Rightarrow p=e=6\)
\(\Rightarrow n=6\)
\(\Rightarrow A=p+n=12\left(C\right)\)
X là Cacbon.
2)
Gọi \(X\left(p_1;e_1;n_1\right)\)\(;Y\left(p_2;e_2;n_2\right)\)\(;Z\left(p_3;e_3;n_3\right)\)
Theo đề, Tổng số electron của \(YZ^{2-}_3\) bằng 32 hạt,
\(\Rightarrow e_2+3e_3+2=32\)
Mà \(p=e\)
\(\Rightarrow p_2+3p_3=30\left(I\right)\)
Y và Z đều có số proton bằng số notron
\(\Rightarrow\left\{{}\begin{matrix}p_2=n_2\\p_3=n_3\end{matrix}\right.\)\(\left(II\right)\)
Hiệu số notron của hai nguyên tố X và Y bằng 3 lần số proton của Z.
\(\Rightarrow n_1-n_2=3p_3\)
\(\Leftrightarrow n_1-p_2-3p_3=0\)\(\left(III\right)\)
\(\left(I\right)-\left(III\right)=>n_1=30\)
Phân tử khối của B bằng 116đvC
\(\Rightarrow p_1+n_1+p_2+n_2+3p_3+3n_3=116\)
\(\Leftrightarrow p_1+n_1+2p_2+6p_3=116\) \(\left(IV\right)\)
\(\left(IV\right)+2\left(III\right)=p_1+3n_1=116\)
\(\Rightarrow p_1=26\)
\(\Rightarrow A_1=p_1+n_1=26+30=56\left(Fe\right)\)
(Đến đây hết dữ kiện để tính Y và Z nên phải biện luận)
Theo (I) ta có: \(p_2+3p_3=30\)
\(\Rightarrow3p_2< 30\)
\(\Leftrightarrow p_2< 10\)
| \(p_2\) | \(1\) | \(2\) | \(3\) | \(4\) | \(5\) | \(6\) | \(7\) | \(8\) | \(9\) |
| \(p_3\) | \(27\) | \(24\) | \(21\) | \(18\) | \(15\) | \(12\) | \(9\) | \(6\) | \(3\) |
=> Chỉ có p2 =8 (O); p3 =6 (C) phù hợp với công thức XYZ3
=> \(\left\{{}\begin{matrix}X:Fe\\Y:C\\Z:O\end{matrix}\right.\)
P/s: Ăn cơm xong rồi làm bài này mất hết 40 phút =="

Câu 2:
Ta có pV = nRT
Với p = 2; V = 0,616 ; R = 0,082; T = 27,3C = 300,3F
\(\rightarrow\)n=\(\frac{2.0,616}{\text{0,082.300,3}}\) = 0,05mol
Câu 3:
a. Tổng số mol khí là : 0,1+0,12+0,05+0,025=0,295mol
\(\rightarrow\)Thể tích khí là 0,295.22,4=6,608l
b. Khối lượng khí X: 0,1.28+0,12.30+0,05.44+0,025.46=9,75g
c. Khối lượng mol của hỗn hợp X: =\(\frac{\text{9,75}}{0,295}\)=33,05
\(\rightarrow\)Tỉ khối so với không khí là \(\frac{33,05}{29}\)=1,139
Câu 1 :Ta có
\(\left\{{}\begin{matrix}\text{8pM+6pX+4nM+3nX=214 }\\\text{8pM+4nM-6pX-3nX=106}\end{matrix}\right.\rightarrow\text{2pM+nM=40}\)
Ta có
pM-3=pX+4
\(\rightarrow\)pM-pX=7
Ta có\(1\le\frac{nM}{pM}\le1,5\)
\(\rightarrow\)\(1\le\frac{40-2pM}{pM}\le1,5\)
\(\rightarrow\) \(11,4\le pM\le13,33\)
\(\rightarrow\left\{{}\begin{matrix}pM=13\\pX=6\end{matrix}\right.\)
\(\rightarrow\) M là Al X là C
\(\rightarrow\)CTHH là Al4C3
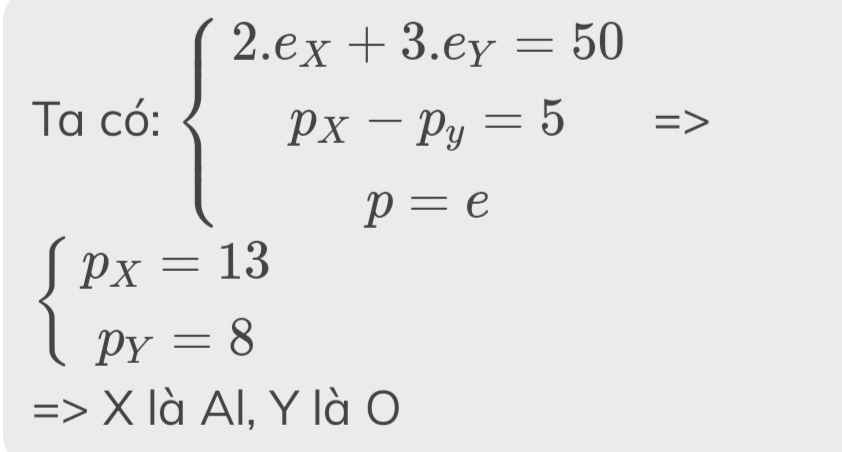
Tổng số proton trong M+ là 11 mà M+ có 5 nguyên tử => số p trung bình của 1 nguyên tử có trong cation M+ là: 11/5 = 2,2
=> Trong M phải có H
Do M+ cấu tạo từ 2 nguyên tố nên gọi M là nguyên tố còn lại trong ion M+ = MnHm
Do M+ có 5 nguyên tử => n + m = 5 => m = 5 - n (1)
Do tổng số proton trong M+ là 11 => pM×n + 1×m = 11 (2)
=> pA×n + 5 - n = 11
=> n(pA - 1) = 6
=> n = 6 / (pA- 1)
=> 1 ≤ 6 / (pA - 1) ≤ 4
=> 2, 5 ≤ pA ≤ 7
Biện luận:
+) pM = 3 => n = 3 , m = 2 => => M+ = ( Li3H2)+ ( loại vì Li có hóa trị I , Hydro có hóa trị I ) . chất LiH thì có, ion LiH+ cũng có.
+) pM = 4 => n = 2 => => M+ = Be2H3+ ( loại vì Be có hóa trị II )
+) pM = 5 => n = 1,5 ( loại : vì không phải số nguyên)
+) pM = 6 => n = 1,2 ( loại : vì không phải số nguyên)
+) pM = 7 => n = 1 ; m= 4 => X+ = NH4+ (nhận)
Gọi Y2−Y2− là AkB2l−AkBl²−
Y(2-) đều do 5 nguyên tử của 2 nguyên tố tạo nên
=> k + l = 5 (3)
2 nguyên tố trong Y²- thuộc cùng 1 nhóm và 2 chu kỳ liên tiếp
=> pA - pB = 8 (4)
tổng số e trong Y²- là 50
=> k×pA + l×pB = 50 - 2 = 48 (5)
=> k×pA + (5 - k)×(pA - 8) = 48
=> k×pA - k×pA - 40 + 8k + 5pA = 48
=> 5pA = 88 - 8k
Biện luận :
+) k = 1 => pA = 16 ; pB = 8 => A = S (nhận) ; B = O => Y²- = SO4²-
+) k = 2 => pA = 14,4 (loại)
+) k = 3 => pA = 12,8 (loại)
+) k = 4 => pA = 11,2 (loại)
Vậy A là (NH4)2SO4