

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án B
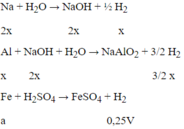
Ta có : a = 0,25V;
còn : x + 3x/2 = 5x/2 = 2,5x = V suy ra x = V/2,5
Vậy a/x = 0,25V/ 0,4V = 5/8

Đáp án B
► Đặt nAl = x; nFe = y ⇒ nNa = 2x ||⇒ Al tan hết ⇒ Y chỉ có Fe.
Bảo toàn electron: nNa + 3nAl = 2nH2 ⇒ 2x + 3.x = 2 × 2 ⇒ x = 0,8 mol.
nFe = nH2 = 0,5 mol ||► nFe : nAl = 0,5 : 0,8 = 5 : 8

Đáp án B
Giả sử số mol Al là x thì số mol Na là 1,25x.
Cho X tác dụng với H2O thì số mol H2 thu được là 2,125x mol.
Z tác dụng với H2SO4 loãng thu được 0,25V lít khí tức 0,53125x mol.
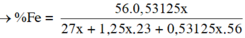
= 74,795 %

Đáp án D
Áp dụng bảo toàn electron có: ![]()
Trường hợp 1: Chất rắn chỉ có Ag
⇒ n Ag = 0 , 7 mol ⇒ m Ag = 75 , 6 gam > 45 , 2 => Loại
Trường hợp 2: Chất rắn có a mol Ag và 2a mol Cu
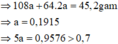
=> Loại =>Ag+ phản ứng hết, Cu2+ phản ứng còn dư
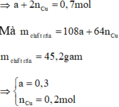

Gọi x là số mol của nhôm trong hỗn hợp X và kV là số mol của khí khi có thể tích V lít. Ta có:
BTe: nNa+3nAl=2n\(H_2\) ⇔ 2x+3x=2kV ⇒ x=nAl=0,4kV.
BTe: 2nFe=2n\(H_2\)=2.0,25kV ⇒ nFe=0,25kV.
Suy ra, \(\dfrac{n_{Fe}}{n_{Al}}=\dfrac{0,25kV}{0,4kV}=\dfrac{5}{8}\).
Chọn D.