Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
BTKL ta có: mX = mdd brom tăng + mY
=> mY = (0,15.16 + 0,09.26 + 0,2.2) – 0,82 = 4,32 (g)
=> nY = 4,32 : 16 = 0,27(mol)
=> VY = 6,048(lit)

Chọn đáp án C
Ta có:mX=0,15.16+ 0,09.26+0,2.2=5,14gam
+ Theo ĐLBTKlg: mX = mY + mZ ⇒ mZ = mX – mY = 5,14 – 0,82 = 4,32 gam.
+ Mà: dZ/H2 = 8 ⇒ MY = 16/
⇒ nZ = mZ ÷ MZ = 4,32 ÷ 16 = 0,27 mol
⇒Thể tích của hh Z: V = 0,27 × 22,4 = 6,048 lít
⇒ Chọn C

nX = 0,1 mol.
Các phản ứng xảy ra:
![]()
Từ tỉ lệ thể tích tính được
![]()
Khối lượng hỗn hợp đầu
![]()
Khối lượng khí thoát ra
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
![]()
Khối lượng bình brom tăng thêm
m1 =m~ m2 = 1,16 - 0,36 = 0,8 gam
Đáp án B.

Đáp án D
Vì hỗn hợp X có nC2H2 = nC2H4
→ quy hh X về C2H3 và H2
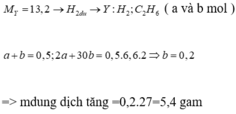

Chọn đáp án C
tính được nH2 = 0,15 mol; n C4H4 = 0,05 mol.
Khi nung nóng thì khối lượng hỗn hợp: msau pư = mtrước pư = 0,15 × 2 + 0,05 ÷ 52 = 2,9 gam.
từ tỉ khối hh sau pư với H2 → n hh sau pư = 2,9 ÷ 2 ÷ 14,5 = 0,1 mol.
Chú ý: nH2 pư = n hh trước pư – n số mol hh sau pư = 0,2 – 0,1 = 0,1 mol.
►Thêm nữa, H2 phản ứng sẽ cộng vào nối đôi, làm mất 0,1 mol liên kết π của hh trước pư.
Mà số mol lk π trước pư là: 0,05 × 3 = 0,15 nên sau phản ứng chỉ còn 0,15 – 0,1 = 0,05 mol π.
Vậy khối lượng brom đã phản ứng sé là: 0,05 × 160 = 8 gam.
Ta chọn đáp án C.

Đáp án A
![]()
![]()
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
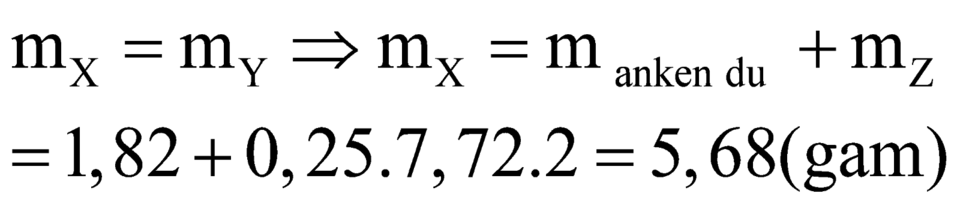
Mà ![]()
![]()
![]()
Do đó hai anken trong X là C2H4 và C3H6.
Cách 1: Áp dụng sơ đồ đường chéo hoặc giải hệ phương trình, ta có:
![]()
Cách 2: Ta có: ![]()
![]()
Vì ![]() nên
nên ![]()

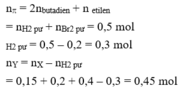
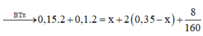
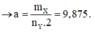
Cho hỗn hợp X qua dung dịch brom dư
thấy hỗn hợp X giảm đi 25% theo thể tích
⇒ nAnkadien = 25% nX
Cho hỗn hợp Y qua dung dịch brom,
thể tích hỗn hợp Y không giảm
⇒ Y gồm Ankan và H2 dư.
⇒ nH2 phản ứng = 2nAnkadien
= 50% nX
⇒ nY = nX – nH2 phản ứng
⇒ nY : nX = 1 : 2
Mà MY = 30 và mY = mX
⇒ MX = 15
Có MX = ( MAnkadien + 3 MH2 ) : 4
⇒ MAnkadien =54
⇒ Ankadien đó là C4H6.
Đáp án A.