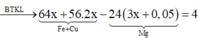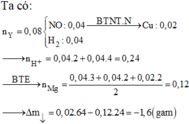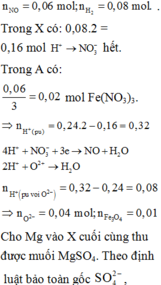Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Từ
Mg + Cu2+ ->Mg2+ + Cu
x x
=> m(tăng) = 64x - 24x = 40x
Mg + 2H+ ->Mg2+ + H2
0,05 0,05
Mg + Fe2+ -> Mg2+ + Fe => m(tăng) = 32.2x
2x 2x 2x
->m(Mgtăng) = 40x + 64x - 1,2 = 4 -> x = 0,05mol
->m(Cu) = 3,2 gam => mCu trong X = 1+3,2=4,2 gam
Lại có
Fe2O3 + 6H+ ->2Fe3+ + 3H2O
x 6x 2x
Cu +2Fe3+->2Fe2+ + Cu2+
x 2x 2x
-> a = 6.0,05:0,4 = 0,75M => Đap an C

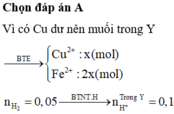
Chọn A
nH+ = 12nN2 + 10nNH4+ + 2nO (oxit) ⇒ nNH4+ = 0,05
Trong dung dịch Y có a mol Mg2+; b mol Fe3+; c mol Fe2+
⇒ nKOH = 2a + 3b + 2c + nNH4+ = 3,15 ⇒ 2a + 3b + 2c = 3,1 (1)
Sau khi tác dụng với KOH thì phần dung dịch chứa 3,15 mol K+; 1,54 mol SO42- và nNO3- = 0,07
Bảo toàn N ⇒ nNO3- ban đầu = 2nN2 + nNH4+ + nNO3- (trong Y) = 0,2
⇒ mX = 24a + 56(b + c) + 62.0,2 + 1,05.16 = 86 (2)
Bảo toàn ne ⇒ 3nAl phản ứng = 3nFe3+ + 2nFe2+ ⇒ nAl phản ứng = b + 2c/3
⇒ mtăng = 56(b + c) – 27(b + 2c/3) = 28 (3)
(1), (2), (3) ⇒ a = 0,15; b = 0,9; c = 0,05
Oxit thu được gồm MgO (0,15 mol) và Fe2O3 (0,95/2 = 0,475) ⇒ m = 0,15.40 + 0,475.160 = 82

C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3
C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑
Y(AgCl, Ag) + HNO3 --> ...
Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O