Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Viết đúng ptpư:
\(Fe+4HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_3\rightarrow2Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(nNO=0,04\left(mol\right)\)
Gọi nFe là x(mol) ; nCu là y(mol)
ta có hệ pt:
\(\left\{{}\begin{matrix}m_{hh}=56x+64y=3,04\\nNO=x+\dfrac{2}{3y}=0,04\end{matrix}\right.\)
Giải hệ ta được: x = 0,02 mol ; y = 0,03 mol
\(\Rightarrow mFe=0,02.56=1,12\left(g\right)\)
\(mCu=0,03.64=1,92\left(g\right)\)

Ta có nNO= 0,15 mol
QT nhận e:
NO3-+ 3e+ 4H+ → NO+ 2H2O
Ta có nNO3- trong muối= ne= 3.nNO= 3.0,15= 0,45 mol
→mmuối nitrat= mkim loại+ mNO3-trong muối= m+ 0,45.62= m+27,9 (gam)
Đáp án D

a)
\(n_{NO} = 0,01(mol)\)
Bảo toàn electron : \(2n_{Cu} = 3n_{NO}\)
\(\Rightarrow n_{Cu} = 0,015(mol)\)
Vậy :
\(\%m_{Cu} = \dfrac{0,01.64}{1,98}.100\% = 32,32\%\\ \%m_{Al_2O_3} = 100\% - 32,32\% = 67,68\%\)
b)
\(n_{Al_2O_3} = \dfrac{1,98-0,015.64}{102} = 0,01(mol)\)
\(n_{OH^-} = n_{NaOH} + 2n_{Ba(OH)_2} = 0,1.1 + 0,5.0,1.2 = 0,2(mol)\)
Ta có :
\(n_{Cu(NO_3)_2} = n_{Cu} = 0,015(mol)\\ n_{Al(NO_3)_3} = 2n_{Al_2O_3} = 0,02(mol)\)
Mà : \(n_{OH^-} = 4n_{Al(NO_3)_3} + 2n_{Cu(NO_3)_2} + n_{HNO_3\ dư}\)
\(\Rightarrow n_{HNO_3\ dư} = 0,09(mol)\)
Bảo toàn nguyên tố với N :
\(n_{HNO_3\ pư} = 3n_{Al(NO_3)_3} + 2n_{Cu(NO_3)_2} = 0,06(mol)\)
Vậy, \(V = \dfrac{0,09 + 0,06}{1} = 0,15(lít)\)

Gọi: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\)
⇒ 56x + 64y = 6,08 (1)
Ta có: \(n_{NO}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
Theo ĐLBT mol e, có: 3x + 2y = 0,08.3 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,04\left(mol\right)\\y=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,04.56}{6,08}.100\%\approx36,8\%\\\%m_{Cu}\approx63,2\%\end{matrix}\right.\)
Bạn tham khảo nhé!

Đáp án A
Trong suốt quá trình số oxi hóa của Al và N thay đổi.

Đáp án A
nNO = 2,8/22,4 = 0,125 (mol)
BTNT N: nNO3 ( trong muối) = 3nNO = 0,375 (mol)
=> mmuối = mKL + mNO3- = 7,55 + 0,375.62 = 30,8 (g)


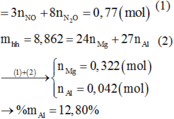
a) nMg:a(mol) ,nAl:b(mol)
nNO=2,464/22,4=0,11(mol)
hpt: mX=24a+27b=3,42
nNO=23a+b=0,11
→a=0,075(mol),b=0,06(mol)
%mMg=(0,075.24/3,42).100%=52,63%
%mAl=100%−52,63%=47,37%
b)
nHNO3=4nNO=0,44(mol)
mdd HNO3=(0,44.63)/10%=277,2(g)