

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

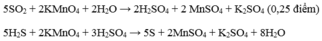

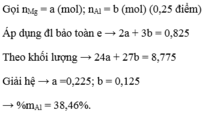

Gọi \(\left\{{}\begin{matrix}n_{Cu}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\left(đk:a,b>0\right)\)
PTHH:
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
a------------------------------->a
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
b----------------------------------->0,5b
\(2NaOH+CuSO_4\rightarrow Cu\left(OH\right)_2\downarrow+Na_2SO_4\)
a---------->a
\(6NaOH+Fe_2\left(SO_4\right)_3\rightarrow2Fe\left(OH\right)_3\downarrow+3Na_2SO_4\)
0,5b----------->a
Theo bài ra, ta có hệ: \(\left\{{}\begin{matrix}160a+400.0,5b=71,2\\98a+107b=40,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0,17\left(mol\right)\\b=0,22\left(mol\right)\end{matrix}\right.\left(TM\right)\)
\(\rightarrow m=0,17.64+0,22.56=23,2\left(g\right)\)

- Chất rắn không tan trong HCL dư là S => m S dư = 3,8g
Kết tủa đen là CuS => n CuS = 0,1 = n H 2 S = nS phản ứng
m S phản ứng = 3,2g
0,2 mol Z gồm 0,1 mol H 2 S và 0,1 mol H 2
m ban đầu = 3,8 + 3,2 = 7g
Ta lại có
n Fe p / u = n S p / u = 0,1 mol
n Fe dư = n H 2 = 0,1 mol
n Fe ban đầu → m Fe ban đầu = 0,2 .56 = 1,12 g
Vậy m = 11,2 + 0,7 = 18,2 (gam)

Coi X là kim loại R có hóa trị n
\(2R + 2nHCl \to 2RCl_n + nH_2\)
Theo PTHH : \(n_R = \dfrac{2}{n}.n_{H_2} = \dfrac{0,3}{n}(mol)\)
\(n_{AgNO_3} = 0,14(mol) ; n_{Cu(NO_3)_2} = 0,1(mol)\)
\(R + nAgNO_3 \to R(NO_3)_n + nAg\\ \)
\(\dfrac{0,14}{n}\).....\(0,14\)............................\(0,14\).................(mol)
\(2R + nCu(NO_3)_2 \to 2R(NO_3)_n + nCu\)
\(\dfrac{0,2}{n}\)......0,1.....................................0.1.............(mol)
Vì \(\dfrac{0,14}{n}\) + \(\dfrac{0,2}{n}\) < \(\dfrac{0,3}{n}\) nên Cu(NO3)2 dư
\(2R + nCu(NO_3)_2 \to 2R(NO_3)_n + nCu\)
\(\dfrac{0,16}{n}\)........0,08....................................0,08...........(mol)
Suy ra : a = 0,14.108 + 0,08.64 = 20,24(gam)