Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Trong X đặt a, b, c lần lượt là số mol FeCl2, Cu, Fe(NO3)2.
Khi cho AgNO3 vào y thì có NO thoát ra
=> Trong Y có H+ dư và NO3- hết, khi đó :
Bảo toàn e : nNO = 2c + 0,02 = ¼ nH+ = 0,1
=> c = 0,04 mol
=> Phần Ag+ phản ứng với Fe2+ = 0,58 – (2a + 0,4)
Khối lượng X = 127a + 64b + 180c = 23,76g
=> a = 0,08 và b = 0,1
=> Muối trong Z gồm : 0,1 mol Cu(NO3)2 và 0,12 mol Fe(NO3)3
=> m = 47,84g

Đáp án C
Chất rắn Y gồm 2 kim loại là Cu và Fe.
Hòa tan hết Y trong HNO3 đặc nóng thu được 0,115 mol NO2.
Gọi số mol Cu và Fe trong Y lần lượt là a, b.
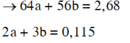
Giải được: a=0,02; b=0,025.
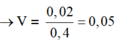
![]()
Gọi số mol Fe, Mg lần lượt là x, y
![]()
Dung dịch X chứa MgSO4 y mol và FeSO4 0,035-y mol(bảo toàn S).
Bảo toàn Fe:
![]()
Giải được: x=0,015; y=0,035.
Cho Ba(OH)2 tác dụng với X thu được kết tủa gồm BaSO4 0,035 mol và Mg(OH)20,035 mol.
Vậy nung kết tủa được rắn nặng m=9,555 gam gồm BaSO4 và MgO

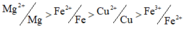
giả thiết cho Y gồm 2 kim loại thì 2 kim loại đó là Fe và Cu.

Do Y chứa Fe nên Cu2+ hết và X chứa MgSO4 và FeSO4.



⇒ kết tủa gồm 0,05 mol BaSO4; 0,025 mol Mg(OH)2; 0,024 mol Fe(OH)2
⇒ rắn khan gồm 0,05 mol BaSO4; 0,025 mol MgO; 0,0125 mol Fe2O3.
m = 0,05.233 + 0,025.40 + 0,0125.160 = 14,65gam
Đáp án B

Đáp án B
Ta nhận thấy mE < mX => KL chưa phản ứng hết; AgNO3 và Cu(NO3)2 hết
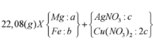
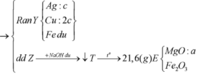
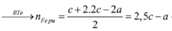
![]()




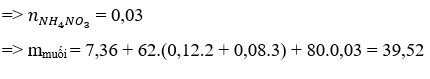
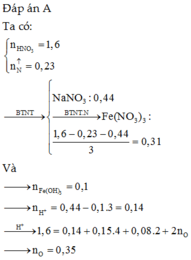
Đáp án C
Hết 0,12 mol NaOH mới có kết tủa chứng tỏ Y có H+. Vậy n(H+) = 0,12 mol
Chất rắn thu được khi cho tác dụng với NaOH là Fe(OH)2 và Fe(OH)3. (Nếu xét chỉ có Fe(OH)2 hay chỉ có Fe(OH)3 thì khối lượng rắn thu được không thỏa mãn)
Y có H+ , có Fe2+ nên NO3- hết.