Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nNaOH/nSO2 = 0.8/1 = 0.8 < 1
=> chỉ có pứ tạo muối axit là NaHSO3, SO2 dư => cô cạn dung dịch ở áp suất nhiệt độ thấp => thu được NaHSO3
Chọn C

FeS + 2HCl => FeCl2 + H2S
H2S + 1/2 O2 thiếu => S + H2O
S + O2 => SO2
SO2 + NaOH => NaHSO3
2NaHSO3 => Na2SO3 + SO2 + H2O
Na2SO3 + SO2 + H2O => 2NaHSO3
NaHSO3 + HCl => NaCl + SO2 + H2O
SO2 + 2NaOH => Na2SO3 + H2O
Na2SO3 + H2SO4 => Na2SO4 + SO2 + H2O
Na2SO4 + BaCl2 => BaSO4 + 2NaCl
NaCl + AgNO3 => AgCl + NaNO3

\(n_{SO_2}=\dfrac{7.84}{22.4}=0.35\left(mol\right)\)
\(n_{NaOH}=0.3\cdot2=0.6\left(mol\right)\)
\(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0.6}{0.35}=1.7\)
=> Tạo ra 2 muối
\(n_{Na_2SO_3}=a\left(mol\right),n_{NaHSO_3}=b\left(mol\right)\)
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
\(NaOH+SO_2\rightarrow NaHSO_3\)
\(BTNa:\) \(2a+b=0.6\)
\(BTS:a+b=0.35\)
\(a=0.25,b=0.1\)
\(m_M=0.25\cdot127+0.1\cdot104=42.4\left(g\right)\)
n NaOH = 0,3.2 = 0,6(mol)
n SO2 = 7,84/22,4 = 0,35(mol)
Ta có :
1 < n NaOH / n SO2 = 0,6/0,35 = 1,7 < 2 nên phản ứng sinh ra : Na2SO3(a mol) , NaHSO3(b mol)
Bảo toàn nguyên tố Na,S :
n NaOH = 2a + b = 0,6(mol)
n SO2 = a + b = 0,35(mol)
=> a = 0,25 ; b = 0,1
=> m muối = 0,25.126 + 0,1.104 = 41,9 gam

Câu10. Hấp thụ hoàn toàn 0.2mol SO2 vào 0,2 mol NaOH. Muối thu được sau phản ứng là:
A.Na2SO3 B.NaHSO4 C.NaHSO3 D.Na2SO3và NaHSO3

Bài 2 :
$n_{HCl} = \dfrac{6,72}{22,4} = 0,3(mol)$
$C\%_{HCl} = \dfrac{0,3.36,5}{50}.100\% = 21,9\%$
Bài 3 :
$a) 2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$b) BaO + H_2SO_4 \to BaSO_4 + H_2O$
$c) 2Na + 2H_2O \to 2NaOH + H_2$
$d) CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
Bài 2:
\(n_{HCl}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\Rightarrow m_{HCl}=0,3.36,5=10,95\left(g\right)\)
\(C\%_{ddHCl}=\dfrac{10,95.100\%}{50}=54,75\%\)
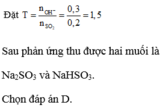

Đáp án D
Số mol các chất là