Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
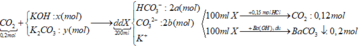
TH1: Nếu trong dd X có OH- dư => dd X chứa OH- dư, CO32-, K+
Khi cho từ từ 100 ml dd X vào 0,15 mol HCl
OH- + H+ → H2O
CO32- + 2H+ → CO2 ↑+ H2O
=> nH+ = nOH- + 2nCO2 > 0,12.2 = 0,24 (mol)
=> loại vì nH+ = 0,15 (mol)
Vậy dd X không chứa OH- dư
TH2: dd X không chứa OH- dư ta có sơ đồ bài toán như trên
Khi cho từ từ 100ml dd X vào 0,15 mol HCl có phản ứng:
HCO3- + H+ → CO2 + H2O
x → x →x (mol)
CO32- + 2H+ → CO2 + H2O
y → 2y → y (mol)

=> a – 3b = 0 (1)
BTNT C: nBaCO3 = a + b = 0,2 (2)
Từ (1) và (2) => a = 0,15 và b = 0,05 (mol)
Trong 200 ml dd X : nHCO3- = 0,3 (mol) ; nCO32- = 0,1 (mol)
Bảo toàn điện tích đối với dd X : nK+ = 0,3 + 0,1.2 = 0,5 (mol)
BTNT C: nCO2(bđ) + nK2CO3 = nHCO3-+ nCO32- => 0,2 + y = 0,3 + 0,1 => y = 0,2 (mol)
BTNT K: nK+ = nKOH + 2nK2CO3 => nKOH = 0,5 – 2.0,2 = 0,1 (mol)
=> x = 0,1 (mol)

Đáp án D
Có n C O 2 b a n đ ầ u = 0,2; n C O 2 s ả n p h ẩ m p h ầ n 1 = 0,12; n B a C O 3 = 0,2
Dung dịch X thu được chứa K2CO3 và KOH dư hoặc K2CO3 và KHCO3
Khi cho 200 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư thu được 0,4 mol kết tủa. Dù thành phần của X gồm những chất nào thì ta luôn có:
n B a C O 3 = n C O 2 b a n đ ầ u + n K 2 C O 3
= 0,2 + y = 0,4 ⇔ y = 0,2
+) Trường hợp 1: Dung dịch X chứa K2CO3 và KOH dư.
Khi đó ở mỗi phần gọi n K 2 C O 3 = a ; n K O H = b
Bảo toàn nguyên tố C, ta có:
2a = n K 2 C O 3 b a n đ ầ u + n C O 2 b a n đ ầ u = 0,4 ⇔ a = 0,2
Khi cho 100ml dung dịch X từ từ vào 300 ml dung dịch HCl 0,5M (0,15 mol HCl) thì xảy ra các phản ứng sau:
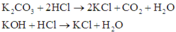
Mà thực tế nHCl < 0,24
Nên trường hợp này không thỏa mãn.
+) Trường hợp 2: Dung dịch X chứa K2CO3 và KHCO3
Khi đó ở mỗi phần gọi n K 2 C O 3 = a ; n K O H = b
Bảo toàn nguyên tố C, ta có:
n B a C O 3 = n K 2 C O 3 + n K H C O 3 = a + b = 0,2 (*)
Khi cho 100ml dung dịch X từ từ vào 300ml dung dịch HCl 0,5M (0,15 mol HCl) thì các phản ứng sau xảy ra đồng thời:
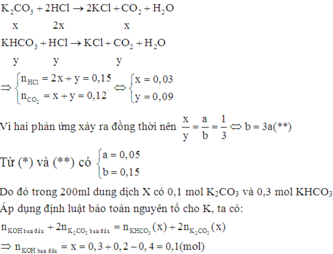

Đáp án B
► Xét TN1: đặt nCO32– phản ứng = a; nHCO3– phản ứng = b.
⇒ nCO2 = a + b = 0,15 mol; nHCl phản ứng = 2a + b = 0,1875 mol
||⇒ giải hệ có: a = 0,0375 mol; b = 0,1125 mol ⇒ nCO32–/X : nHCO3–/X = a : b = 1 : 3.
► Xét TN2: ∑nC/X = n↓ = 0,25 mol ⇒ 250 ml X chứa 0,5 mol C.
Bảo toàn nguyên tố Cacbon: y = 0,5 – 0,25 = 0,25 mol.
● Chia 0,5 mol C thành 0,125 mol CO32– và 0,375 mol HCO3–.
Bảo toàn điện tích: nK+ = 0,625 mol. Bảo toàn nguyên tố Kali:
x = 0,625 – 0,25 × 2 = 0,125 mol

Đáp án D
Khi cho từ từ HCl và X, đã có phương trình tạo khí
H+ + HCO3- → CO2 + H2O
Dung dịch Y không thể chứa OH- , CO32-. Vậy Y chứa KCl 0,5 mol (BTNT cho Cl) và KHCO3 y mol.
Cho y phản ứng với Ba(OH)2 dư:
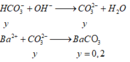
ĐLBKL cho K ta có n(KOH) ban đầu = 0,4x= 0,5 +y = 0,7 => y = 1,75

Đáp án D
Nhỏ từ từ axit vào dung dịch X ⇒ dung dịch Y.
⇒ Y chứa KCl và KHCO3.
Cho Y + dung dịch Ba(OH)2 dư ⇒ có phản ứng.
KHCO3 + Ba(OH)2 → BaCO3 + KOH + H2O.
+ Mà nKHCO3 = nBaCO3 = 0,2 mol.
+ Bảo toàn Cl ⇒ nKCl = nHCl = 0,5 mol.
⇒ Bảo toàn K ⇒ nKOH = nKCl + nKHCO3 = 0,7 mol.
⇒ CM KOH = 0 , 7 0 , 4 = 1,75M

Đáp án D
Nhỏ từ từ axit vào dung dịch X ⇒ dung dịch Y.
⇒ Y chứa KCl và KHCO3.
Cho Y + dung dịch Ba(OH)2 dư ⇒ có phản ứng.
KHCO3 + Ba(OH)2 → BaCO3 + KOH + H2O.
+ Mà nKHCO3 = nBaCO3 = 0,2 mol.
+ Bảo toàn Cl ⇒ nKCl = nHCl = 0,5 mol.
⇒ Bảo toàn K ⇒ nKOH = nKCl + nKHCO3 = 0,7 mol.
⇒ CM KOH = 0 , 7 0 , 4 = 1,75M

Đáp án A
Ta có: n C O 2 = 0,35 mol; nNaOH = 0,2.2 = 0,4 mol
→ T = n N a O H n C O 2 = 0 , 4 0 , 35 = 1 , 14
→ Tạo 2 muối
CO2+ NaOH → NaHCO3
x x x mol
CO2+ 2NaOH →Na2CO3+ H2O
y 2y y mol
Ta có: n C O 2 = x+y = 0,35 mol; nNaOH = x+2y = 0,4 mol
→x = 0,3 và y = 0,05
Dung dịch X chứa 0,3 mol NaHCO3 và 0,05 mol Na2CO3
Trong 100 ml dung dịch Y có: nHCl = 0,1 mol; n H 2 S O 4 = 0,1x mol
→ n H + = 0,1+ 0,2x mol; n S O 4 2 - = 0,1x mol
Cho từ từ 100 ml dung dịch Y vào 200 ml dung dịch X thu được n C O 2 = 0,25 mol
H++ CO32- → HCO3-
0,05←0,05→ 0,05
H+ + HCO3- → CO2+ H2O
0,25 0,25← 0,25 mol
Ta có:
n H + = 0,05+ 0,25 = 0,1+ 0,2x → x = 1 mol/l
Dung dịch Z có chứa Na+ ; HCO3- ; SO42-: 0,1x = 0,1 mol
Ba2+ + SO42- → BaSO4 ↓
n B a S O 4 = n S O 4 2 - = 0,1 mol → m B a S O 4 = 0,1.233 = 23,3 gam


Đáp án A