
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(S_{NaNO_3\left(50^oC\right)}=114\left(g\right)\)
=> Ý nghĩa là ở 50oC thì có thể hoà tan 114 g NaNO3 vào 100 g nước
b, \(S_{NaCl\left(36^oC\right)}=42\left(g\right)\)
=> Ý nghĩa là ở 36oC thì có thể hoà tan 42 g NaCl vào 100 g nước

a) Giả sử lấy 100 gam dung dịch NaOH 30%
=> \(m_{NaOH}=100.30\%=30\left(g\right)\)
Sau khi thêm nước ta được dung dịch 10%
=>C%= \(\dfrac{30}{100+m_{H_2O}}=10\%\)
=> mH2O = 200 (g)
Vậy tỉ lệ : \(\dfrac{m_{H2O}}{m_{ddNaOH30\%}}=\dfrac{200}{100}=2\)
b) Sau khi cô cạn :
\(m_{dd}=\dfrac{m_{NaOH}}{50\%}=\dfrac{30}{50\%}=60\left(g\right)\)
Ta có : \(\dfrac{m_{dd}}{m_{ddNaOH30\%}}=\dfrac{60}{100}=0,6\)
Vậy cần cô cạn dung dịch giảm 0,6 lần thì được dung dịch 50%

2) bạn tự học SGK
3) nP = 3,1/31 = 0,1 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
Mol: 0,1 ---> 0,125
2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,125 . 2 = 0,25 (mol)
mKMnO4 = 0,25 . 158 = ,39,5 (g)


Câu 2:
\(1,4P+5O_2\xrightarrow{t^o}2P_2O_5\\ 2,2Fe+3Cl_2\xrightarrow{t^o}2FeCl_3\\ 3Al_2O_3+3H_2SO_4\to Al_2(SO_4)_3+3H_2O\\ 4,2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\\ 5,2Al(OH)_3\xrightarrow{t^o}Al_2O_3+3H_2O\\ 6,Al_2O_3+3H_2SO_4\to Al_2(SO_4)_3+3H_2O\\ 7,4Na+O_2\to 2Na_2O\\ 8,C_nH_{2n-2}+\dfrac{3n-1}{2}O_2\xrightarrow{t^o}nCO_2\uparrow+(n-1)H_2O\)

Fe2O3 + 3CO --to--> 2Fe + 3CO2
Theo ĐLBTKL: mCO + mFe2O3 = mFe + mCO2
=> mFe = 32 + 16,8 - 26,4 = 22,4 (kg)

Câu 8.
a.b.
\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,2 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
\(m_{AlCl_3}=0,2.133,5=26,7g\)
c.\(n_{CuO}=\dfrac{8}{80}=0,1mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,1 < 0,3 ( mol )
0,1 0,1 ( mol )
\(m_{Cu}=0,1.64=6,4g\)
Câu 9.
a.b.
\(n_{Zn}=\dfrac{16,25}{65}=0,25mol\)
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,25 < 0,6 ( mol )
0,25 0,5 0,25 0,25 ( mol )
Chất dư là HCl
\(m_{HCl\left(dư\right)}=\left(0,6-0,5\right).36,5=3,65g\)
\(m_{ZnCl_2}=0,25.136=34g\)
c.\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,25 0,25 ( mol )
\(m_{Cu}=0,25.64.90\%=14,4g\)


 giúp mik câu 3 và 4 với, mik cảm ơn
giúp mik câu 3 và 4 với, mik cảm ơn

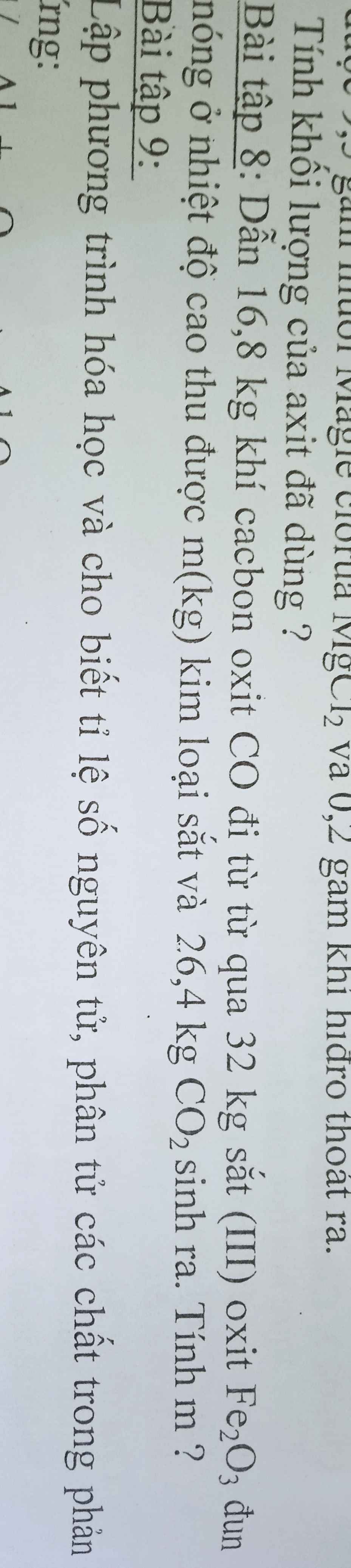



\(a,n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,2--------------->0,2------>0,2
\(H_2+CuO\xrightarrow[]{t^o}Cu+H_2O\)
0,2-------------->0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\\ b,m_{ZnCl_2}=0,2.136=27,2\left(g\right)\\ c,m_{Cu}=0,2.64=12,8\left(g\right)\)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(L\right)\\ m_{ZnCl_2}=136.0,2=27,2\left(g\right)\)
\(pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,2 0,2
\(m_{Cu}=0,2.64=12,8\left(g\right)\)