Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

theo bài ta có:nH2=6,72/22,4=0,3(mol)
pthh; 2Al+3H2SO4------>Al2(SO4)3+3H2 (1)
2Al2O3+3H2SO4-------->Al2(SO4)3+3H2O (2)
ta có:nAl=0,3(mol)
=>mAl=0,3*27=8,1(g)
=>mAl2O3=15,6-8,1=7,5(g)
=>nAl2O3=7,5/102=5/68(mol)
=>nH2SO4=1,5*0,3+1,5*5/68=0,56(mol)
=>V(H2SO4)=0,56/1,5=0,37(l)
Chúc bạn học tốt![]()

a, PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_{Al}=\dfrac{2}{3}n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,1.27}{5,25}.100\%\approx51,43\%\\\%m_{Al_2O_3}\approx48,57\%\end{matrix}\right.\)
b, \(n_{Al_2O_3}=\dfrac{5,25-0,1.27}{102}=0,025\left(mol\right)\)
Theo PT: \(n_{HCl}=3n_{Al}+6n_{Al_2O_3}=0,45\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{0,45.36,5}{29,2\%}=56,25\left(g\right)\)
c, \(n_{H_2SO_4}=\dfrac{1}{2}n_{HCl}=0,225\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,225.98}{19,6\%}=112,5\left(g\right)\)

PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
a_______a________a______a (mol)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
b_______\(\dfrac{3}{2}\)b_________\(\dfrac{1}{2}\)b_____\(\dfrac{3}{2}\)b (mol)
a) Ta lập HPT: \(\left\{{}\begin{matrix}24a+27b=8,25\\a+\dfrac{3}{2}b=\dfrac{2,24}{22,4}=0,1\end{matrix}\right.\) \(\Leftrightarrow\) Hệ có nghiệm âm
*Bạn xem lại đề !!!

a/ PTHH: 2Al + 3H2SO4 ===> Al2(SO4)3 + 3H2
0,2 0,3 0,3
MgO + H2SO4 ===> MgSO4 + H2O
0,1 0,1
nH2 = 6,72 / 22,4 = 0,3 mol
=> nAl = 0,2 mol
=> mAl = 0,2 x 27 = 5,4 gam
=> mMgO = 9,4 - 5,4 = 4 gam
=> %mAl = \(\frac{5,4}{9,4}.100\%=57,45\%\)
%mMgO = 100% - 57,45% = 42,55%
b/ nMgO = 4 / 40 = 0,1 mol
Lập các số mol theo phương trình, ta có:
\(\sum nH2SO4\) = 0,1 + 0,3 = 0,4 mol
=> mH2SO4 = 0,4 x 96 = 38,4 gam
=> mdung dịch H2SO4 19,6% = 38,4 : 19,6% = 195,92 gam

150ml = 0,15l
Số mol của kali hidroxit
CMKOH = \(\dfrac{n}{V}\Rightarrow n=C_M.V=0,2.0,15=0,03\left(mol\right)\)
Pt : K2O + H2O \(\rightarrow\) 2KOH\(|\)
1 1 2
0,015 0,03
a) Số mol của kali oxit
nK2O = \(\dfrac{0,03.1}{2}=0,015\left(mol\right)\)
Khối lượng của kali oxit
mK2O= nK2O . MK2O
= 0,015 . 94
= 1,41 (g)
Khối lượng của đồng (II) oxit
mCuO = 13 - 1,41
= 11,59 (g)
b) 0/0K2O = \(\dfrac{m_{K2O}.100}{m_{hh}}=\dfrac{1,41.100}{13}=10,85\)0/0
0/0CuO = \(\dfrac{m_{CuO}.100}{m_{hh}}=\dfrac{11,59.100}{13}=89,15\)0/0
c) Có : mCuO = 11,59 (g)
số mol của đồng (II) oxit
nCuO = \(\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{11,59}{80}=0,14\left(mol\right)\)
Pt : CuO + H2SO4 → CuSO4 + H2O\(|\)
1 1 1 1
0,14 0,14
K2O + H2SO4 → K2SO4 + H2O\(|\)
1 1 1 1
0,015 0,015
Số mol tổng của axit sunfuric
nH2SO4 = 0,14 + 0,015
= 0,155 (mol)
Khối lượng của axit sunfuric
mH2SO4 = nH2SO4 . MH2SO4
= 0,155 . 98
= 15,19 (g)
Khối lượng của dung dịch axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{15,19.100}{20}=\) 75,95 (g)
Thể tich của dung dịch axit sunfuric cần dùng
D = \(\dfrac{m}{V}\Rightarrow V=\dfrac{m}{D}=\dfrac{75,95}{1,143}=66,45\left(ml\right)\)
Chúc bạn học tốt

a) \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,1 0,1 0,1
PTHH: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Mol: 0,05 0,05
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow m_{Fe_2O_3}=13,6-5,6=8\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
b và c ko hiểu đề
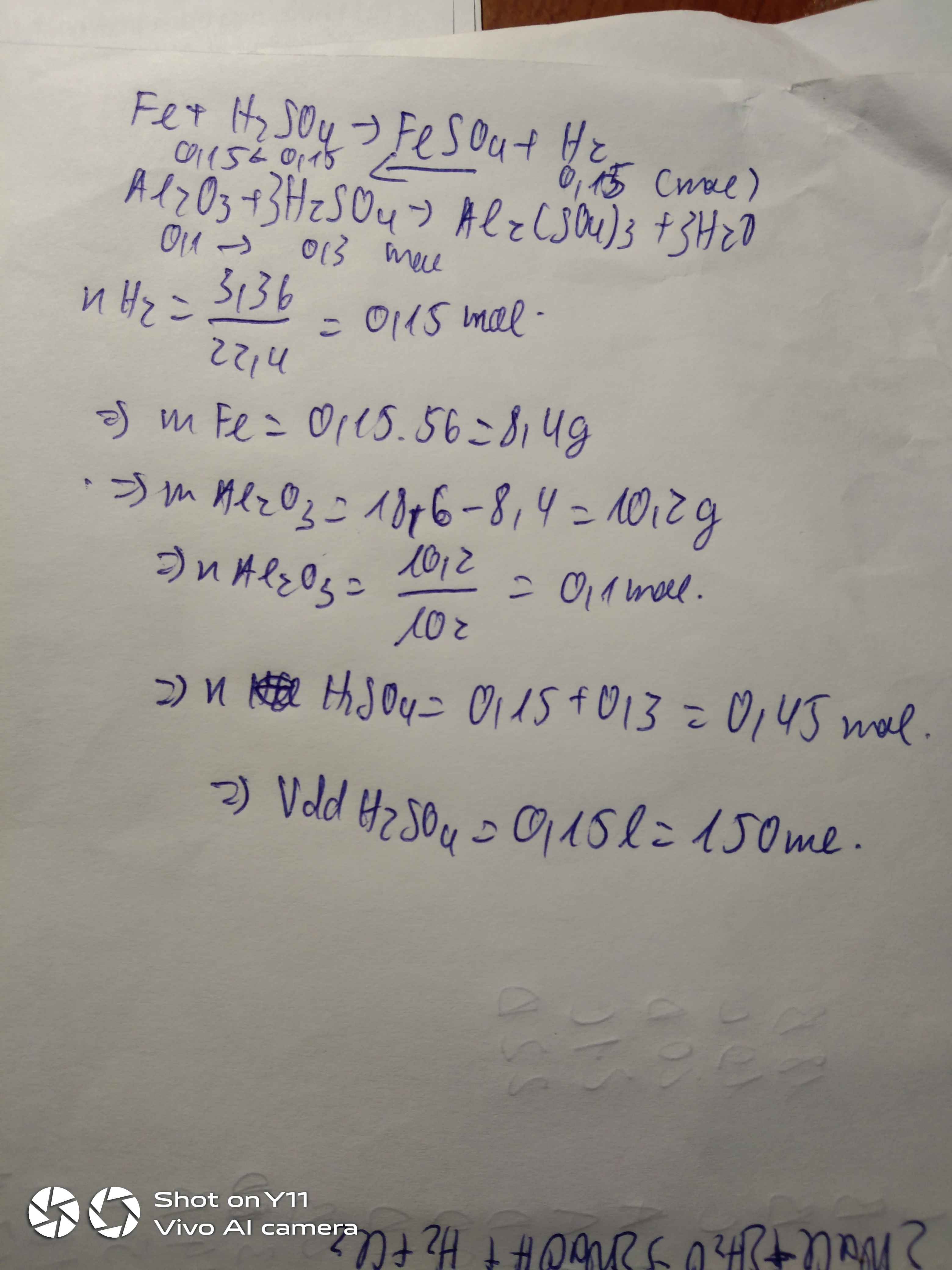
đề sai r