
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


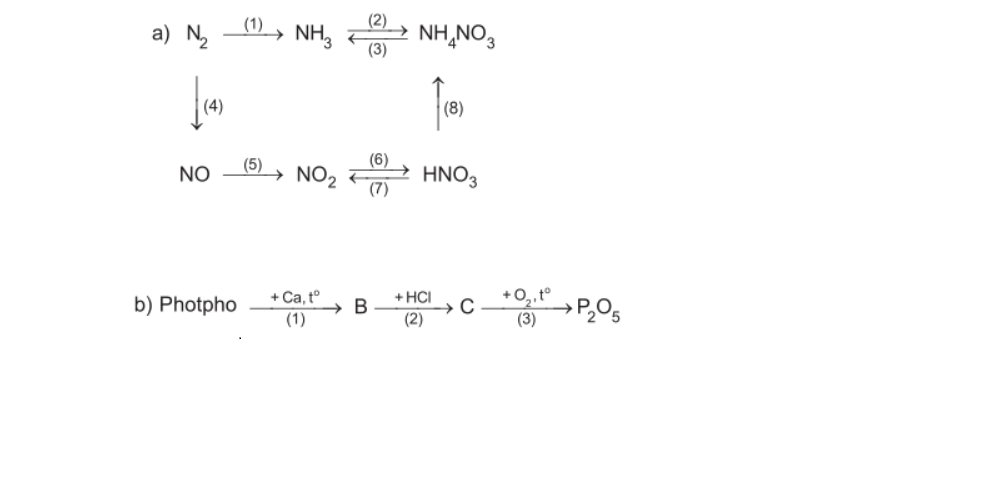
a)
\(\left(1\right)N_2+3H_2⇌\left(xt,t^o,P\right)2NH_3\\ \left(2\right)NH_3+HNO_3\rightarrow NH_4NO_3\\ \left(3\right)NH_4NO_3+KOH\rightarrow KNO_3+NH_3+H_2O\\ \left(4\right)N_2+O_2⇌\left(3000^oC\right)2NO\\ \left(5\right)2NO+O_2\rightarrow2NO_2\\ \left(6\right)4NO_2+O_2+2H_2O\rightarrow4HNO_3\\ \left(7\right)Cu+4HNO_{3\left(đ\right)}\underrightarrow{t^o}Cu\left(NO_3\right)_2+2NO_2+2H_2O\\ \left(8\right)NH_3+HNO_3\rightarrow NH_4NO_3\)
b)
\(\left(1\right)2P+3Ca\underrightarrow{to}Ca_3P_2\\ \left(2\right)Ca_3P_2+6HCl\rightarrow3CaCl_2+2PH_3\\ \left(3\right)2PH_3+4O_2\underrightarrow{to}P_2O_5+3H_2O\)
Lưu ý đối với các phản ứng 2 chiều, mình không có thêm được điều kiện trên mũi tên phản ứng (do đặc thù của latex hoc24.vn) vì thế mình có mở ngoặc sau, bạn nào sau này thấy thì trong ngoặc là đk phản ứng nhé!

CnH2n-2 +\(\frac{3n-1}{2}\)O2==>nCO2 +(n-1)H2O
CO2 +Ca(OH)2==>CaCO3 + H20
n CaCO3=0.2(mol)
Có nCo2=nCaCO3=0.2(mol)và nCO2=nnhân mol của ankin
==>0.2=n\(\frac{2.7}{14n-2}\)==>n=4
CTPT:C4H6
b,Do chỉ thu được 1 sp ==>CTCT:CH3-C=C-CH3(ở giữa là lk 3 nhé em, anh không biết vẽ lk 3 trên máy tính


PTHH: 3Cu + 8HNO3 ----> 3Cu(NO3)2 + 2NO + 4H2O (1)
0,45mol 0,3 mol
CuO + 2HNO3 ---------> Cu(NO3)2 + H2O
Ta có n NO = 6,72/22,4 = 0,3 mol
Theo pthh (1): n Cu = 0,45 mol
=> m Cu = 0,45 . 64 = 28,8 g
=> m CuO = 30 - 28,8 = 1,2 g
n NO = 0,3 mol --> n Cu = 0,3*3/2 = 0,45 mol --> m Cu=28,3 gam --> m CuO = 1,2 gam

vd 10 :
CH3COOH ↔ CH3COO- + H+
ban đầu: 0,1
phản ứng 0,1α 0,1α 0,1α
cân bằng : 0,1 - 0,1α 0,1α 0,1α
=> nồng độ mol của H+ và CH3COO- nhé
câu kia bạn làm tương tự


 Giúp em 2 câu cuối với
Giúp em 2 câu cuối với
 c bác giải giúp em câu 21 đc không ạ? em đang bị mất kiến thức hoá nên có thể có lời giải cụ thể càng tốt ạ. em cảm ơn
c bác giải giúp em câu 21 đc không ạ? em đang bị mất kiến thức hoá nên có thể có lời giải cụ thể càng tốt ạ. em cảm ơn




17)
a)
\(CH_3-CH_3\underrightarrow{t^o,xt}CH_2=CH_2+H_2\)
\(CH_2=CH_2+Br_2\rightarrow CH_2Br-CH_2Br\)
\(CH_2Br-CH_2Br+2KOH\underrightarrow{ancol,t^o}CH\equiv CH+2KBr+2H_2O\)
\(CH\equiv CH+H_2O\underrightarrow{HgSO_4,H_2SO_4}CH_3CHO\)
b)
\(CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+CH\equiv CH\)
\(2CH\equiv CH\underrightarrow{đime.hóa}CH\equiv C-CH=CH_2\)
\(CH\equiv C-CH=CH_2+H_2\underrightarrow{t^o,Pd/PbCO_3}CH_2=CH-CH=CH_2\)
\(nCH_2=CH-CH=CH_2\underrightarrow{t^o,p,Na}\left(-CH_2-CH=CH-CH_2-\right)_n\)
c)
\(Al_4C_3+12H_2O\rightarrow4Al\left(OH\right)_3+3CH_4\)
\(2CH_4\underrightarrow{1500^oC,làm.lạnh.nhanh}CH\equiv CH+3H_2\)
\(CH\equiv CH+H_2\underrightarrow{t^o,Pd/PbCO_3}CH_2=CH_2\)
\(CH_2=CH_2+H_2O\underrightarrow{t^o,H_2SO_4}CH_3-CH_2OH\)
\(CH_3-CH_2OH+3O_2\underrightarrow{t^o}2CO_2+3H_2O\)
d)
\(CH_3-CH_2OH\underrightarrow{170^oC,H_2SO_4}CH_2=CH_2+H_2O\)
\(CH_2=CH_2+HCl\rightarrow CH_3-CH_2Cl\)
\(CH_3-CH_2Cl+KOH\underrightarrow{t^o,ancol}CH_2=CH_2+KCl+H_2O\)
\(nCH_2=CH_2\underrightarrow{t^o,p,xt}\left(-CH_2-CH_2-\right)_n\)
\(\)
18)
- Trích một ít các chất làm mẫu thử
a)
- Cho các khí tác dụng với dd AgNO3/NH3
+ Không hiện tượng: C2H6, C2H4 (1)
+ Kết tủa vàng: C2H2
\(C_2H_2+2AgNO_3+2NH_3\rightarrow C_2Ag_2+2NH_4NO_3\)
- Dẫn các khí còn lại ở (1) tác dụng với dd Br2 dư:
+ dd nhạt màu dần: C2H4
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
+ Không hiện tượng: C4H10
b)
- Dẫn các khí qua dd AgNO3/NH3:
+ Không hiện tượng: C4H10, \(CH_3-C\equiv C-CH_3\) (1)
+ Kết tủa vàng: \(CH\equiv C-CH_2-CH_3\)
\(CH\equiv C-CH_2-CH_3+AgNO_3+NH_3\rightarrow CAg\equiv C-CH_2-CH_3\downarrow+NH_4NO_3\)
- Dẫn các khí còn lại ở (1) tác dụng với dd Br2 dư
+ dd nhạt màu dần: \(CH_3-C\equiv C-CH_3\)
\(CH_3-C\equiv C-CH_3+2Br_2\rightarrow CH_3-CBr_2-CBr_2-CH_3\)
+ Không hiện tượng: C2H6
c)
- Dẫn các khí qua dd AgNO3/NH3:
+ Kết tủa vàng: \(CH\equiv C-CH_3\)
\(CH\equiv C-CH_3+AgNO_3+NH_3\rightarrow CAg\equiv C-CH_3\downarrow+NH_4NO_3\)
+ Không hiện tượng: C2H6, \(CH_2=CH-CH=CH_2\) (1)
- Dẫn các khí còn lại ở (1) tác dụng với dd Br2 dư
+ dd nhạt màu dần: \(CH_2=CH-CH=CH_2\)
\(CH_2=CH-CH=CH_2+2Br_2\rightarrow CH_2Br-CHBr-CHBr-CH_2Br\)
+ Không hiện tượng: C2H6