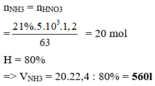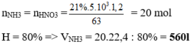Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Các phương trình điều chế HNO3 từ NH3
4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
2NO + O2→ 2NO2
4NO2 + O2 + 2H2O→ 4HNO3
Theo bảo toàn nguyên tố N ta có:
nNH3= nHNO3=0,05.0,1=5.10-3 mol
→ VNH3=0,112 lít=112 ml

Đáp án C
Các phương trình điều chế HNO3 từ NH3
4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
2NO + O2→2NO2
4NO2 + O2 + 2H2O→ 4HNO3
Theo bảo toàn nguyên tố N ta có:
nHNO3=nNH3=112 000/22,4=5000 mol
→mHNO3=315 000 gam= 315 kg
→ mddHNO3= 315.100/60=525 kg
Do hiệu suất bằng 80% nên mddHNO3 thực = mPT.80/100= 525.80/100=420 kg

Đáp án A
Theo bảo toàn nguyên tố N ta có;
nHNO3= nNH3= 2 mol → mHNO3=126 gam
Do hiệu suất mỗi phản ứng lần lượt là 60%; 50%; 80% nên
mHNO3 thực tế thu được= 126. 60%.50%.80%= 30,24 gam

Đáp án C
Khối lượng N có trong phân đạm là 100.34%= 34 kg= 34 000 gam
→nN= 17 000/7 mol
NH3+ HNO3→ NH4NO3
Đặt nNH3= nHNO3= x mol→ bảo toàn nguyên tố N ta có:
nN= x+ x= 17 000/7 → x=8500/7 mol
→mNH3= 20642 gam= 20,6 kg
và mdd HNO3 45%= (8500/7).63.100/45=170 000 gam= 170 kg

Hiệu suất của cả quá trình là: 90%.90%.90% = 72,9%
Theo PTHH,cứ 1 mol NH3 thì tạo ra 1 mol HNO3
=> Cứ 17g NH3 thì tạo ra 63g HNO3
=> Cứ 17g NH3 thì tạo ra 100g dd HNO3 63%
=> Cứ 51kg NH3 thì tạo ra 300kg HNO3 63%
=> Khối lượng dd HNO3 63% thực tế là \(\dfrac{300.72,9}{100}=218,7\left(kg\right)=218700\left(g\right)\)