Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Oxit kim loại M : \(M_xO_y\)
\(n_{O(oxit)} = n_{CO_2} = n_{CaCO_3} = \dfrac{8}{100} = 0,08(mol)\)
Bảo toàn nguyên tố với O:
\(n_{oxit} = \dfrac{n_O}{y} = \dfrac{0,08}{y}mol\\ \Rightarrow \dfrac{0,08}{y}(Mx + 16y) = 4,64\\ \Leftrightarrow \dfrac{0,08Mx}{y} = 3,36 \)
Với x = 3 ; y = 4 thì M = 56(Fe)
(Đáp án C)
Đáp án là Fe, oxit là Fe3O4
Loại bỏ Al, Zn do Co không khử được oxit của nó.
Thử máy tính cho thấy Cuo không thỏa mãn -->FexOy
8g kết tủa--> 0.08mol O
Số mol FexOy= 4.64/(56x+16y)=0.08y. Biến đổi x theo y
Lần lượt cho y=2,3, 8/3 (hóa trị của Fe) sẽ tìm dc y (y là số tự nhiên dương phù hợp)

Chọn đáp án B.
F e + C u S O 4 → F e S O 4 + C u ( i ) 3 C O + F e 2 O 3 → t o 3 C O 2 + 2 F e ( j ) 2 N a C l + 2 H 2 O → c ó m à n g n g ă n đ i ệ n p h â n 2 N a O H + C l 2 + H 2 ( k ) 3 F e + 3 O 2 → t o 2 F e 2 O 3 ( l ) 3 A g + 4 H N O 3 → 3 A g N O 3 + N O + 2 H 2 O ( m ) 2 C u ( N O 3 ) 2 → t o 2 C u O + 4 N O 2 + O 2 ( n ) 2 F e 3 O 4 + 10 H 2 S O 4 → t o 3 F e 2 ( S O 4 ) 3 + S O 2 + 10 H 2 O ( o ) F e C O 3 → t o F e O + C O 2
Các thí nghiệm xảy ra sự oxi hóa kim loại: (a), (d), (e).

Đáp án B
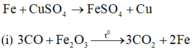
(j) 2NaCl + 2 H 2 O → c ó m à n g n g ă n đ i ệ n p h â n 2NaOH + C l 2 + H 2
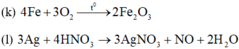
![]()
(n) 2 F e 3 O 4 + 10 H 2 S O 4 → 3 F e 2 ( S O 4 ) 3 + S O 2 + 10 H 2 O
![]()
Các thí nghiệm xảy ra sự oxi hóa kim loại: (a), (d), (e).

Đáp án C
(a) Đúng vì tại catot ( - ) c ó 2 H 2 O + 2 e → 2 O H - + H 2
(b) Đúng
(c) Sai vì Fe mạnh hơn Ni trong dãy điện hóa nên xảy ra ăn mòn Fe
(d) Đúng vì C u + F e 2 S O 4 3 → C u S O 4 + 2 F e S O 4 → tách Ag ra khỏi hỗn hợp Ag và Cu
(e) Sai vì chỉ tạo muối F e N O 3 2

Đáp án C
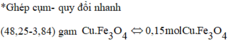
→ 48,24 gam hỗn hợp ban đầu gồm 0,15 mol Fe 3 O 4 và (0,15 + 3,84 : 64 = 0,21 mol) Cu.
Sơ đồ gộp quá trình:
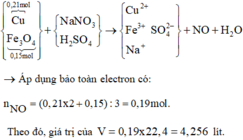

Chọn C.
Mg.