Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức chung của hỗn hợp X là CnH2n+2-2k
\(n_{CO_2}=0,2n\left(mol\right)\)
\(n_{H_2O}=\dfrac{0,2.\left(2n+2-2k\right)}{2}=0,1\left(2n+2-2k\right)=0,2n+0,2-0,2k\left(mol\right)\)
=> 0,2n + 0,2 - 0,2k = 0,2n + 0,02
=> k = 0,9
=> CTPT: CnH2n+0,2
PTHH: CnH2n+0,2 + 0,9Br2 --> CnH2n+0,2Br1,8
0,1------>0,09
=> \(V_{dd.Br_2}=\dfrac{0,09}{1}=0,09\left(l\right)\)

Gọi \(\left\{{}\begin{matrix}n_{CO}=a\left(mol\right)\\n_{C_nH_{2n+2}}=b\left(mol\right)\end{matrix}\right.\)
=> \(a+b=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Bảo toàn C: \(a+bn=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Bảo toàn H: \(2bn+2b=\dfrac{2,7}{18}.2=0,3\left(mol\right)\)
=> a = 0,15; b = 0,05; n = 2
=> CTPT: C2H6
\(\left\{{}\begin{matrix}\%V_{C_2H_6}=\dfrac{0,05}{0,2}.100\%=25\%\\\%V_{CO}=\dfrac{0,15}{0,2}.100\%=75\%\end{matrix}\right.\)

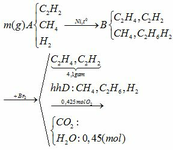
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)

a. \(n_X=\dfrac{V_{O_2}}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{CO_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
+ Bảo toàn C:
\(\Rightarrow n_{CH_4}+2n_{C_2H_4}=0,3\left(mol\right)\)
Mà: \(n_{CH_4}+n_{C_2H_4}=0,2\left(mol\right)\)
\(\Rightarrow0,2+n_{C_2H_4}=0,3\)
\(\Leftrightarrow n_{C_2H_4}=0,3-0,2=0,1\left(mol\right)\)
Phần trăm theo thể tích từng khí X là:
\(\%V_{C_2H_4}=\dfrac{0,1.100\%}{0,2}=50\%\)
\(\%V_{C_2H_4}=100\%-50\%=50\%\)
b. Bảo toàn H
\(\Rightarrow n_H=4n_{CH_4}+4n_{C_2H_4}\)
\(\Leftrightarrow n_H=4\left(n_{CH_4}+n_{C_2H_4}\right)\)
\(\Leftrightarrow n_H=4\left(0,1+0,1\right)\)
\(\Leftrightarrow n_H=4.0,2=0,8\left(mol\right)\)
\(\Rightarrow n_{H_2O}=\dfrac{n_H}{2}=\dfrac{0,8}{2}=0,4\left(mol\right)\)
Khối lượng nước thu được:
\(\Rightarrow m_{H_2O}=n_{H_2O}.M_{H_2O}=0,4.18=7,2\left(g\right)\)

a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,5\left(mol\right)\\n_{C_2H_2}=1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,5.22,4}{33,6}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=3,5\left(mol\right)\Rightarrow m_{O_2}=3,5.32=112\left(g\right)\)

a, PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Ta có: \(n_{CH_4}+n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{H_2O}=2n_{CH_4}+n_{H_2}=\dfrac{16,2}{18}=0,9\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,4\left(mol\right)\\n_{H_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,4.22,4}{11,2}.100\%=80\%\\\%V_{H_2}=20\%\end{matrix}\right.\)
b, Theo PT: \(n_{CO_2}=n_{CH_4}=0,4\left(mol\right)\Rightarrow V_{CO_2}=0,4.22,4=8,96\left(l\right)\)

\(n_{CO_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\); \(n_{O_2}=\dfrac{10,64}{22,4}=0,475\left(mol\right)\)
BTKL: mCO2 + mH2O = 8,3 + 0,475.32 = 23,5 (g)
=> nH2O = \(\dfrac{23,5-0,35.44}{18}=0,45\left(mol\right)\)
=> nH = 0,9 (mol)
nC = 0,35 (mol)
=> \(n_O=\dfrac{8,3-0,35.12-0,9.1}{16}=0,2\left(mol\right)\)
Giả sử X chứa CnH2n+2Ox, Cn+1H2n+4Oy
Đặt \(\left\{{}\begin{matrix}n_{C_nH_{2n+2}O_x}=a\left(mol\right)\\n_{C_{n+1}H_{2n+4}O_y}=b\left(mol\right)\end{matrix}\right.\)
Bảo toàn C: an + bn + b = 0,35
=> 2an + 2bn + 2b = 0,7 (1)
Bảo toàn H: 2an + 2a + 2bn + 4b = 0,9 (2)
Bảo toàn O: ax + by = 0,2 (3)
(2) - (1) => 2a + 2b = 0,2 => a + b = 0,1
(1) => 2n(a+b) + 2b = 0,7
=> 0,2n + 2b = 0,7
Mà 0 < b < 0,1
=> 2,5 < n < 3,5
=> n = 3
Vậy X chứa C3H8Ox, C4H10Oy
=> \(\left\{{}\begin{matrix}a+b=0,1\\3a+4b=0,35\end{matrix}\right.\)
=> a = 0,05 (mol); b = 0,05 (mol)
Thay vào (3)
=> 0,05x + 0,05y = 0,2
=> x + y = 4
TH1: x = 1; y = 3
=> X chứa C3H8O, C4H10O3
TH2: x = 2; y = 2
=> X chứa C3H8O2, C4H10O2
TH3: x = 3; y = 1
=> X chứa C3H8O3, C4H10O
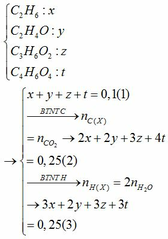
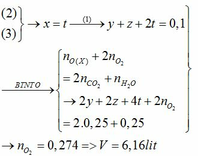
nx1 = nx2 = V/22.4 (1)
PTHH
C3H8 + 5O2---> 3CO2 +4H2O. (1)
Bảo toàn số mol ==>n C3H8 = n H2O - nCO2 (2)
2H2 + O2 ==> 2H2O (2)
theo pt n H2 = nH2O (3)
lấy 2 + 3 ==> nC3H8 + nH2= nA = sum (nH2O ) - nCO2 =1.3a -1a = 0.3a (4)
lấy (1) - (4) ==> n C2H4 trong X1 =nC2H4 trong X2 =V/22.4 - 0.3a (mol)
Vì n C2H4 trong X1 =nC2H4 trong X2 và số mol CO2 và H2O sinh ra ở 2 pt là như nhau nên bảo toàn số mol
==> n C3H8 + nH2 trong X1 = n ankan trong X2
hay 0.3a mol = n ankan trong X2
vậy khi đốt cháy 0.3 a mol C3H8+H2 (trong X1) cũng là đốt 0.3a mol ankan trong X2
hay đốt 1mol C3H8 +H2 trong X1 giống đốt 1mol ankan trong X2
đặt CT HH cho ankan đó là CnH2n+2 (1 mol)
CnH2n+2 + (3n+1)/2 O2 --> n CO2 + n+1 H2O (3)
đặt a là số mol C3H8 Pứ pthh(1)
b là số mol H2 pứ pthh(2)
vì nC3H8 +nH2 trong X1 = n ankan trong X2 (chứng minh trên kia)
nên ta có hệ: hông biết lập hệ thôg cảm
a+b =1mol
và nCO2(1)=nCO2 (3)
hay 3a= n ×1 = n
cho n chạy từ 1 đến 4
n = 1 ==> CH4 ==> a = 1/3 ==> b = 2/3 mol
n=2. ===> C2H6 ==>a=2/3 mol ==> b=1/3 mol
n=3 ==> C3H8 ==> a =1mol ==> b=0 mol loại
n=4 ==> C4H10 ==> a= 4/3 loại
vậy ankan a là CH4 và C2H6
chúc may mắn nè
like ủng hộ mình nhé
Có: \(n_{X_1}=n_{X_2}=\frac{V}{22,4}\)
\(n_{C_3H_8}+n_{H_2}=n_A=n_{H_2O}-n_{CO_2}=0,3a\)
\(\rightarrow n_{C_2H_4trongX_1}=n_{C_2H_4trongX_2}=\frac{V}{22,4}-0,3a\)
\(\rightarrow\) Đốt cháy 0,3 mol C3H8 + H2 giống đốt cháy 0,3 mol A ( CnH2n + 2)
\(\rightarrow\) Đốt cháy 1 mol ( C3H8 + H2 ) giống đốt cháy 1 mol C2H2n + 2
\(\rightarrow n< 3\)
\(\rightarrow A\) là CH4 hoặc C2H6