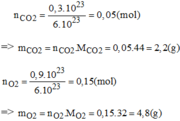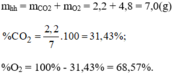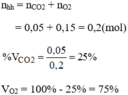Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Thành phần theo khối lượng:
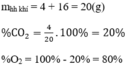
Thành phần phần trăm theo thể tích:


Khối lượng của các khí:
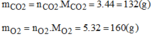
Thành phần phần trăm theo khối lượng:
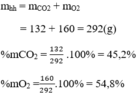
Thành phần phần trăm theo thể tích:
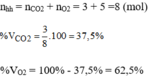

tham khảo
Ta có: dA/O2=¯¯¯¯¯¯¯¯MA32=1,25⇒¯¯¯¯¯¯¯¯MA=32.1,25=40(∗)dA/O2=MA¯32=1,25⇒MA¯=32.1,25=40(∗)
Phương trình phản ứng : C+O2→CO2(1)C+CO2→2CO(2)C+O2→CO2(1)C+CO2→2CO(2)
Bài toán này có thể xảy ra hia trường hợp sau :
Trường hợp 1 : Oxi dư (không có phản ứng 2) : Hỗn hợp A gồm CO2 và O2 dư. Thành phần phần trăm các chất trong hỗn hợp về mặt toán học không ảnh hưởng đến số mol hỗn hợp. Xét 1 mol hỗn hợp A, trong đó X là số mol của CO2 và (1-x) là số mol của O2 dư.
Ta có ¯¯¯¯¯¯¯¯MA=44x+(1–x)321=40⇒x=23MA¯=44x+(1–x)321=40⇒x=23
Vậy %VCO2=23.100=66,67%%VCO2=23.100=66,67%
%VO2=33,33%.%VO2=33,33%.
Trường hợp 2 : O2 thiếu (có phản ứng 2), hỗn hợp A có CO2 và CO.
Tương tự trên, xét 1 mol hỗn hợp A, trong đó A là số mol của CO2 và (1-a) là số mol của CO.
Ta có : ¯¯¯¯¯¯¯¯MA=44x+(1–x)281=40⇒x=0,75MA¯=44x+(1–x)281=40⇒x=0,75
Vậy %VCO2=aa+b.100=3b4b.100=75%%VCO2=aa+b.100=3b4b.100=75%
%VCO=25%.%VCO=25%.
b) Tính m, V.
CO2+Ca(OH)2→CaCO3↓+H2O0,06←0,06=6100CO2+Ca(OH)2→CaCO3↓+H2O0,06←0,06=6100
Trường hợp 1 : nCO2=0,06mol⇒nO2dư=0,03(mol)nCO2=0,06mol⇒nO2dư=0,03(mol)
Vậy mc=0,06.12=0,72gammc=0,06.12=0,72gam
VO2=(0,06+0,03).22,4=2,016VO2=(0,06+0,03).22,4=2,016(lít)
Trường hợp 2 : nCO2=0,06mol,nCO=13nCO2=0,02(mol)nCO2=0,06mol,nCO=13nCO2=0,02(mol)
⇒nC=nCO2+nCO=0,06+0,02=0,08⇒mC=0,08.12=0,96(g)nO2=nCO2+12nCO=0,06+0,01=0,07mol⇒VO2=0,07.22,4=1,568(lit)⇒nC=nCO2+nCO=0,06+0,02=0,08⇒mC=0,08.12=0,96(g)nO2=nCO2+12nCO=0,06+0,01=0,07mol⇒VO2=0,07.22,4=1,568(lit)

a)
dA/O\(_2\) = \(\dfrac{M_A}{32}\) = 1,25 \(\Rightarrow\) MA = 32 . 1,25 = 40
PTPƯ: C + O2 -----> CO2
C + CO2 -----> 2CO
Trường hợp 1 (Oxi dư)
Ta có: MA = \(\dfrac{44x+\left(1-x\right).32}{1}\) = 40 \(\Rightarrow\) x = \(\dfrac{2}{3}\)
Vậy %VCO\(_2\) = \(\dfrac{2}{3}\) . 100 = 66,67%
%VO\(_2\) = 33,33%
Trường hợp 2 (Oxi thiếu)
MA = \(\dfrac{44x+\left(1-x\right).28}{1}\) = 40 \(\Rightarrow\) x = 0,75
Vậy % VCO\(_2\) = \(\dfrac{a}{a+b}\) . 100 = \(\dfrac{3b}{4b}\) . 100 = 75%
%VCO = 25%
b)
CO2 + CA(OH)2 -----> CaOH3 \(\downarrow\) + H2O
0,06 \(\leftarrow\) 0,06 = \(\dfrac{6}{100}\)
Trường hợp 1 (nCO\(_2\) = 0,06 mol \(\Rightarrow\) nO\(_2\) dư = 0,03 mol)
Vậy mc = 0,06.12 = 0,75 (g)
VO\(_2\) = (0,06 + 0,03) . 22,4 = 2,016 (l)
Trường hợp 2 (nCO\(_2\) = 0,06 mol, nCO = \(\dfrac{1}{3}\) nCO\(_2\) = 0,02 mol)
\(\Rightarrow\) nC = nCO\(_2\) + nCO = 0,06 + 0,02 = 0,08 (mol)
\(\Rightarrow\) mC = 0,08 . 12 = 0,96 (g)
nO\(_2\) = nCO\(_2\) + \(\dfrac{1}{2}\) nCO = 0,06 + 0,01 = 0,07 (mol)
VO\(_2\) = 0,07.22,4 = 1,568 (l)
cho mình hỏi tại sao ở câu b th 1 no2 dư = 0,03 với còn th 2 thì nco = 1/3 nco2

a) Gọi số mol Al, Zn là 2a, a (mol)
PTHH: 4Al + 3O2 --to--> 2Al2O3
2a-->1,5a---------->a
2Zn + O2 --to--> 2ZnO
a---->0,5a------->a
=> \(102a+81a=18,3\)
=> a = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{0,2.27+0,1.65}.100\%=45,378\%\\\%m_{Zn}=\dfrac{0,1.65}{0,2.27+0,1.65}.100\%=54,622\%\end{matrix}\right.\)
b) \(n_{O_2}=1,5a+0,5a=0,2\left(mol\right)\)
=> \(V_{O_2}=0,2.22,4=4,48\left(l\right)\)

a. Ag không phản ứng nên ta có PTHH: \(2Mg+O_2\rightarrow^{t^o}2MgO\)
\(\rightarrow m_{O_2}=m_{hh}-m_{\mu\text{ối}}=18,8-15,6=3,2g\)
\(\rightarrow n_{O_2}=\frac{3,2}{32}=0,1mol\)
b. \(\rightarrow V_{O_2}=n.22,4=22,4.0,1=2,24l\)
\(\rightarrow V_{kk}=4,48.5=11,2l\)
c. Có \(n_{Mg}=2n_{O_2}=0,2l\)
\(\rightarrow m_{Mg}=0,2.24=4,8g\)
\(\rightarrow\%m_{Mg}=\frac{4,8.100}{15,6}\approx30,77\%\)
\(\rightarrow\%m_{Ag}=100\%-30,77\%=69,23\%\)