Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$n_{CO_2} = \dfrac{11,2}{22,4} = 0,5(mol)$
$n_{H_2O} = \dfrac{14,4}{18} = 0,8(mol)$
$\Rightarrow$ Hai hidro cacbon có CTTQ là $C_nH_{2n+2}$
$n_{2\ hidrocacbon} = n_{H_2O} - n_{CO_2} = 0,3(mol)$
Suy ra số mol của 2 hidrocacbon lần lượt là 0,1 ; 0,2
Gọi số C của hai hidrocacbon là n , m
Bảo toàn C, ta có : $0,1n + 0,2m = 0,5$
Với n = 1 ; m = 2 thì thỏa mãn
Vậy hai hidrocacbon là $CH_4,C_2H_6$
Đáp án A
Bạn thiếu trường hợp nhé vì ở đây tỉ lệ 1:2 không rõ là CH4 với HĐC hay HĐC với CH4. Đáp án phải là D

nCO2 = 0,2
nH2O = 0,3
nH2O > nCO2 ⇒ 2 Hidrocacbon đó là ankan
Gọi công thức chung của 2 chất đó là CnH2n+2 (n>1)
Ta có n CO2 : n H2O = n : (n+1) = 0,2 : 0,3 ⇒ n = 2
⇒ 2 chất đó là CH4 và C3H8
Đáp án D.

CTPT: CxHy
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> \(n_{C_xH_y}=\dfrac{0,3}{x}\left(mol\right)\)
=> \(M_{C_xH_y}=12x+y=\dfrac{4,4}{\dfrac{0,3}{x}}\left(g/mol\right)\)
=> \(\dfrac{x}{y}=\dfrac{3}{8}\)
=> C3H8 thỏa mãn
=> B

Đáp án A
nX = 0,1 mol; nH2O = 0,35 mol
nX = nH2O - nCO2 => nCO2 = 0,35 - 0,1 = 0,25 mol
→ V = 22,4.0,25 = 5,6 lít

Gọi \(\left\{{}\begin{matrix}n_{CO_2}=a\left(mol\right)\\n_{H_2O}=b\left(mol\right)\end{matrix}\right.\)
\(m_{giảm}=m_{BaCO_3}-m_{CO_2}-m_{H_2O}\)
=> 44a + 18b = 29,5 (1)
Bảo toàn C; nC = a (mol)
Bảo toàn H: nH = 2b (mol)
=> 12a + 2b = 6,3 (2)
(1)(2) => a = 0,425 (mol); b = 0,6 (mol)
Do \(n_{CO_2}< n_{H_2O}\)
=> 2 hidrocacbon là ankan
nankan = 0,6 - 0,425 = 0,175 (mol)
=> \(\overline{C}=\dfrac{0,425}{0,175}=2,43\)
Mà 2 ankan liên tiếp nhau
=> 2 ankan là C2H6 và C3H8

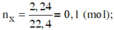
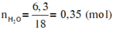
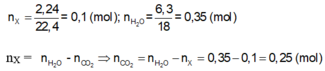
nCO2 = 0,25
nH2O = 0,35
nH2O > nCO2 ⇒ 2 Hidrocacbon đó là ankan
Gọi công thức chung của 2 chất đó là CnH2n+2 (n>1)
Ta có n CO2 : n H2O = n : (n+1) = 0,25 : 0,35 ⇒ n = 2,5
⇒ 2 chất đó là C2H6 và C3H8