Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án là C
Đốt: nước vôi trong dư nên 25,5 gam kết tủa
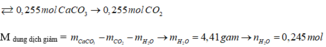
Lại có X gồm C + H + O mà m X = 4 , 03 g a m → n O = 0 , 03 m o l
X dạng ( R C O O 3 ) C 3 H 5 → n X = 0 , 005 m o l
Vậy với 8,06 gam X (dùng gấp đôi trên) thì
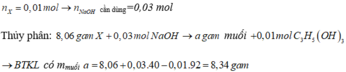

Chọn đáp án C
Ta có:
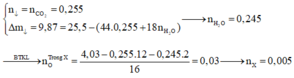
→ B T K L 8 , 06 + 0 , 01 . 3 . 40 = a + 0 , 01 . 92 → a = 8 , 34 g a m

4,03 gam X + O2 → CO2 + H2O
Đưa sản phẩm qua bình đựng nước vôi trong nCO2 = nCaCO3 = 0,255 mol
mdd giảm = mkết tủa - mH2O – mCO2 → 25,5 - mH2O - 0,255.44 = 9,87 → nH2O = 0,245 mol
→ X có nC = nCO2 = 0,255 mol và nH = 2nH2O = 2.0,245 =0,49 mol
→ nO = (4,03 - 0,255.12 - 0,49.1)/16 = 0,03 mol
Vì X là triglixerit nên X có 6 O trong CTPT → nX = 0,005
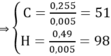
→ X: C51H98O6
Xét 8,06 g X + NaOH → muối + glixerol thì
nX = 8,06/(12.51 + 98.1 + 16.6) = 0,01 → nNaOH = 3nX = 0,03 mol và nglixerol = nX = 0,01 mol
Bảo toàn khối lượng có mmuối = mX + mNaOH – mglixerol = 8,06 + 0,03.40 – 0,01 .92 =8,34 g
Đáp án cần chọn là: A

Chọn đáp án D
Giải bài tập (CO2; H2O) cho vào dung dịch Ca(OH)2 dư.
![]() mol.
mol.
![]()
![]()
⇒ ![]() mol
mol
⇒ đốt 4,03 gam X → 0,255 mol CO2 + 0,245 mol H2O.
Có ![]() gam
gam
⇒ nO trong X = 0,03 mol.
X là triglixerit
→ nX = ![]() ÷ 6 = 0,005 mol.
÷ 6 = 0,005 mol.
⇒ tỉ lệ, khi dùng 8,06 gam X
⇔ có 0,01 mol X.
Phản ứng: X + 3NaOH → muối + 1C3H3(OH)3 (glixerol).
⇒ có ![]() = 0,03 mol
= 0,03 mol
nglixerol sinh ra = nX = 0,01 mol.
⇒ bảo toàn khối lượng có
m = mmuối = 8,06 + 0,03 × 40 – 0,01 × 92 = 8,34 gam

Chọn đáp án D
giải bài tập (CO2; H2O) cho vào dung dịch Ca(OH)2 dư.
có nCO2 = nCaCO3↓ = 0,255 mol.
mdung dịch giảm = mCaCO3 – ∑(mCO2 + mH2O) ⇒ mH2O = 4,41 gam
⇒ nH2O = 0,245 mol ||⇒ đốt 4,03 gam X → 0,255 mol CO2 + 0,245 mol H2O.
có mX = mC + mH + mO ⇒ mO = 0,48 gam ⇒ nO trong X = 0,03 mol.
X là triglixerit → nX = ∑nO trong X ÷ 6 = 0,005 mol.
⇒ tỉ lệ, khi dùng 8,06 gam X ⇔ có 0,01 mol X.
Phản ứng: X + 3NaOH → muối + 1C3H5(OH)3 (glixerol).
⇒ có nNaOH cần = 3nX = 0,03 mol và nglixerol sinh ra = nX = 0,01 mol.
⇒ bảo toàn khối lượng có m = mmuối = 8,06 + 0,03 × 40 – 0,01 × 92 = 8,34 gam.

Đáp án C
Theo định luật bảo toàn khối lượng ta có:
mEste? + mNaOH? = mMuối✓ + mAncol✓
Khi đốt muối của axit no đơn chức mạch hở ta có phản ứng:
2CnH2n–1O2Na + (3n–2)O2 → t o Na2CO3 + (2n–1)CO2 + (2n–1) H2O.
⇒ nCO2 = nH2O Û mDung dịch giảm = mCaCO3 – mCO2 – mH2O.
Đặt nCO2 = nH2O = a ⇒ 100a – 44a – 18a = 3,42 Û a = 0,09 mol.
+ Từ phản ứng đốt muối ta có tỷ lệ:
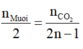 .
.
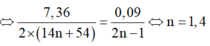
⇒ nMuối = 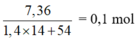 = nNaOH pứ
= nNaOH pứ
⇒ nNaOH pứ = 4 gam ✓.
+ Bảo toàn
khối lượng ⇒ mEste = 7,36 + 3,76 – 4 = 7,12 gam

Đáp án C
Ta có: MX < 160
Cho 13,8 gam X tác dụng với NaOH được dung dịch cô cạn thu được rắn Y có khối lượng 22,2 gam.
Đốt cháy Y thu được 0,15 mol Na2CO3 và hỗn hợp khí Z.
Dẫn Z qua bình nước vôi trong thu được 0,25 mol kết tủa CaCO3 và dung dịch T.
Đun dung dịch thu được thêm 0,15 mol kết tủa nữa.
Do vậy T chứa 0,15 mol Ca(HCO3)2
→ n C O 2 = 0 , 25 + 0 , 15 . 2 = 0 , 55 m o l
Dung dịch thu được có khối lượng tăng lên so với ban đầu là 3,7 gam
→ m C O 2 + m H 2 O - m C a C O 3 = 3 , 7 → n H 2 O = 0 , 25 m o l
Bảo toàn nguyên tố Na suy ra số mol NaOH là 0,3 mol.
Bảo toàn khối lượng: m H 2 O = 13 , 8 + 0 , 3 . 40 - 22 , 2 = 3 , 6 → n H 2 O = 0 , 2
Bảo toàn nguyên tố C: nO trong X = 0,55 + 0,15 = 0,7 mol
Bảo toàn nguyên tố H: nH trong X = 0,25.2 + 0,2.2-0,3 = 0,6 mol
=> n O t r o n g X = 13 , 8 - 0 , 7 . 12 - 0 , 6 16 = 0 , 3
Do vậy trong X tỉ lệ C:H:O=7:6:3 nên CTPT của X có dạng (C7H6O3)n
mà theo giả thiết đầu nên n phải bằng 1.
Vậy X là C7H6O3.
=> nX =0,1 mol
Vậy X tác dụng với NaOH theo tỉ lệ 1:3 và sinh ra 2H2O nên CTCT của X dạng HCOOC6H4OH.
X tác dụng được với nước brom vừa đủ sẽ tạo thành HO-CO-O-C6H4-x(OH)(Br)x
→ 80 x 61 + 12 . 6 + 4 x + 17 + 80 x = 51 , 282 % → x = 2 như vậy sẽ chỉ có 2Br được thế nằm ở trên vòng.ư
Do đó vị trí của nhóm chức HCOO- trên vòng so với HO- là sẽ ở vị trí o hoặc p.
Do vậy có 2 đồng phân cấu tạo phù hợp với X.

Đáp án là C
Ta có
mX=13.8 , MX <160
X + NaOH thu được Y
Y + O2 => ![]() = 0.15
= 0.15
=> nNaOH =0.3 và Z
Z + Ca(OH)2 ta có phương trình:
m tăng thêm + m kết tủa 1= 28.7 g
= ![]()
Tổng mol 2 lần kết tủa là 0.55 = số mol của CO2
=> nC trong X= 0.55+0.15=0.7 mol
Suy ra mol H2O = 0.25 mol
Ta có phương trình
X + NaOH ![]() Y + H2O
Y + H2O
Bảo toàn khối lượng
![]() = 0.2 mol
= 0.2 mol
Bảo toàn H ta có
nH trong X = 0.2*2+ 0.25*2 – 0.3= 0.6 mol
Suy ra ta tính được nO trong X=( 18.96-0.6-0.7*12) /16= 0.3
Suy ra công thức đơn giản nhất trùng với công thức phân tử của X là C7H6O3
Do X tác dụng với Br2 ra % Br=51.282% ứng với công thức C7H4O3Br2
X có 4 π trong phân tử và tác dụng với 3 mol NaOH nên X là este của HCOOH với C6H4(OH)2
Suy ra công thức cấu tạo X được 2 cái ( OH ở vị trí octo hoặc para vì chỉ tác dụng được với 2 Br2)
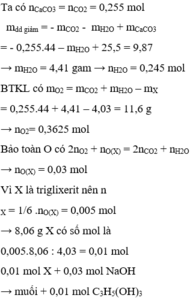
Chọn đáp án C