Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. Khi đốt cháy A ta thu được C02 và H20; vậy A phải chứa C và H.
Khối lượng C trong 1,792 lít C02 là : 12.1,79222,412.1,79222,4 = 0,96 (g).
Khối lượng H trong 1,44 g H20 : 2.1,44182.1,4418 = 0,16 (g).
Đó cũng là khối lượng C và H trong 3,96 g A.
Theo đầu bài A phải chứa Cl. Khối lượng Cl trong 7,175 g AgCl :
35,5.7,175143,5=1,775(g)35,5.7,175143,5=1,775(g)
Đó cũng là khối lượng Cl trong 2,475 g A.
Vậy, khối lượng Cl trong 3,96 g A : 1,775.3,962,4751,775.3,962,475 = 2,840 (g).
Khối lượng C, H và Cl đúng bằng khối lượng chất A (3,96 g).
Vậy, chất A có dạng CxHyClz.
x : y : z = 0,9612:0,161:2,8435,50,9612:0,161:2,8435,5 = 0,08 : 0,16 : 0,08 = 1 : 2 : 1
CTĐGN của A là CH2Cl.
2. MA = 3,3.30 = 99 (g/mol)
⇒(CH2Cl)n⇒(CH2Cl)n = 99 ⇒⇒ 49,5n = 99 ⇒⇒ n = 2
CTPT của A là C2H4Cl2.
3. Các CTCT
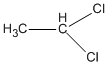 1,1-đicloetan
1,1-đicloetan
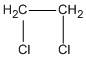 1,2-đicloetan (etylen clorua)
1,2-đicloetan (etylen clorua)

1. Theo định luật bảo toàn khối lượng:
m A = m C O 2 + m H 2 O − m O 2
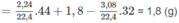
Khối lượng C trong 1,8 g A là: 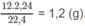
Khối lượng H trong 1,8 g A là: 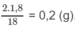
Khối lượng O trong 1,8 g A là : 1,8 - 1,2 - 0,2 = 0,4 (g).
Công thức chất A có dạng C x H y O z :
x : y : z = 0,1 : 0,2 : 0,025 = 4 : 8 : 1
CTĐGN là C 4 H 8 O
2. M A = 2,25.32 = 72 (g/mol)
⇒ CTPT trùng với CTĐGN: C 4 H 8 O .
3. Các hợp chất cacbonyl C 4 H 8 O :
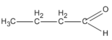 (butanal)
(butanal)
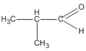 (2-metylpropanal)
(2-metylpropanal)
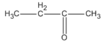 (butan-2-ol)
(butan-2-ol)

1. CTĐGN là C 7 H 8 O
2. CTPT là C 7 H 8 O
3. Có 5 CTCT phù hợp :
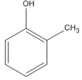 (2-metylphenol (A1))
(2-metylphenol (A1))
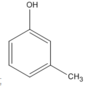 (3-metylphenol (A2))
(3-metylphenol (A2))
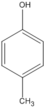 (4-metylphenol (A3))
(4-metylphenol (A3))
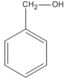 (ancol benzylic (A4))
(ancol benzylic (A4))
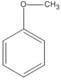 ( metyl phenyl ete (A5))
( metyl phenyl ete (A5))
4. Có phản ứng với Na: A1, A2, A3, A4;
Có phản ứng với dung dịch NaOH: A1, A2, A3.

1. C 2 H 4 O .
2. Số mol A trong 1,10 g A = số mol O 2 trong 0,40 g O 2
n
O
2

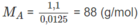
( C 2 H 4 O ) n = 88 ⇒ 44n = 88 ⇒ n = 2
CTPT là C 4 H 8 O 2 .

Ta có: \(d_{A/H_2}=100\)
\(\Rightarrow M_A=100.2=200\left(g/mol\right)\)
\(\Rightarrow n_A=\dfrac{2}{200}=0,01\left(mol\right)\)
\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\Rightarrow n_C=0,1\left(mol\right)\)
⇒ Số nguyên tử C trong A là: \(\dfrac{0,1}{0,01}=10\)
\(n_{H_2O}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\Rightarrow n_H=0,08.2=0,16\left(mol\right)\)
⇒ Số nguyên tử H trong A là: \(\dfrac{0,16}{0,01}=16\)
Giả sử n là số nguyên tử O có trong A.
Ta có: 10.12 + 16 + n.16 = 200
⇒ n = 4
Vậy: CTPT của A là C10H16O4.
Bạn tham khảo nhé!
Bảo toàn nguyên tố với C,H :
\(n_C = n_{CO_2} = \dfrac{4,4}{44}= 0,1(mol)\\ n_H = 2n_{H_2O} = 2.\dfrac{1,792}{22,4} = 0,16(mol)\)
Mà :
\(m_O = m_A - m_C - m_H = 2 - 0,1.12 - 0,16 = 0,64(gam)\\ \Rightarrow n_O = \dfrac{0,64}{16} = 0,04(mol)\)
Ta có :
\(n_C: n_H : n_O = 0,1 :0,16 : 0,04 = 5 : 8 : 2\)
Vậy CTPT của A là : \((C_5H_8O_2)_n\)
Mà :
\(M_A = (12.5+8+16.2)n = M_{H_2}.100 = 200(đvC)\\ \Rightarrow n = 2\)
Vậy CTPT của A : \(C_{10}H_{16}O_4\)

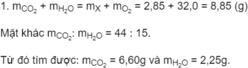
Khối lương C: 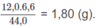
Khối lượng H: 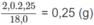
Khối lượng O: 2,85 - 1,80 - 0,25 = 0,80 (g).
Chất X có dạng CxHyOz
x : y : z = 0,150 : 0,25 : 0,050 = 3 : 5 : 1
Công thức đơn giản nhất của X là C 3 H 5 O .
2, M X = 3,80 x 30,0 = 114,0 (g/mol)
( C 3 H 5 O ) n = 114; 57n = 114 ⇒ n = 2.
Công thức phân tử C 6 H 10 O 2 .

1. Số mol
C
O
2
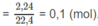
Số mol
H
2
O
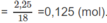
Khi đốt ancol A, số mol H 2 O tạo thành < số mol C O 2 . Vậy A phải là ancol no, mạch hở. A có dạng C n H 2 n + 2 - x ( O H ) x hay C n H 2 n + 2 O x .
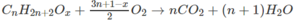
Theo đầu bài ta có:
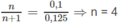
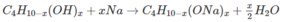
Theo phương trình : Cứ (58 + 16x) g A tạo ra 0,5000x mol H 2 .
Theo đầu bài:
Cứ 18,55 g A tạo ra 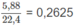 mol
H
2
.
mol
H
2
.
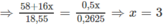
CTPT của A là C 4 H 10 O 3 .
Theo đầu bài A có mạch cacbon không nhánh; như vậy các CTCT thích hợp là
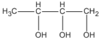 (butan-1,2,3 triol)
(butan-1,2,3 triol)
Và 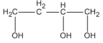 (butan-1,2,4-triol)
(butan-1,2,4-triol)
2. Để tạo ra 0,1 mol C O 2 ;
Số mol A cần đốt là: 
Như vậy: m = 0,025 x 106 = 2,65 (g).

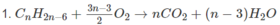
Cứ ( 14n - 6) g A tạo ra n mol C O 2
Cứ 1,50 g A tạo ra 
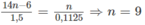
Công thức phân tử của A là C 9 H 12
2. Các công thức cấu tạo
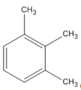 (1,2,3-trimetylbenzen )
(1,2,3-trimetylbenzen )
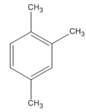 (1,2,4-trimetylbenzen)
(1,2,4-trimetylbenzen)
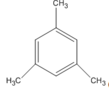 (1,3,5-trimetylbenzen)
(1,3,5-trimetylbenzen)
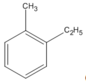 (1-etyl-2-metylbenzen)
(1-etyl-2-metylbenzen)
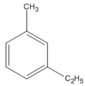 (1-etyl-3-metylbenzen)
(1-etyl-3-metylbenzen)
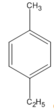 (1-etyl-4-metylbenzen)
(1-etyl-4-metylbenzen)
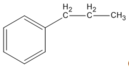 (propylbenzen)
(propylbenzen)
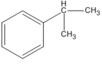 (isopropylbenzen)
(isopropylbenzen)
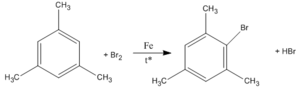
3. 

1. 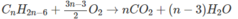
Theo phương trình:
Cứ (14n - 6)g A tác dụng với 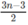 mol
O
2
mol
O
2
Theo đầu bài:
Cứ 13,24g A tác dụng với 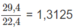 mol
O
2
mol
O
2
Ta có 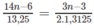
⇒ n = 8 ⇒ CTPT: C 8 H 10
2. Các công thức cấu tạo
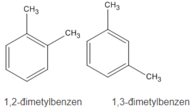
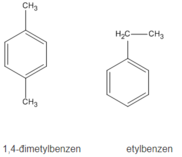
1. Khi đốt cháy A ta thu được C O 2 và H 2 O ; vậy A phải chứa C và H.
Khối lượng C trong 1,792 lít C O 2 là: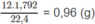
Khối lượng H trong 1,44 g H 2 O :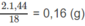
Đó cũng là khối lượng C và H trong 3,96 g A.
Theo đầu bài A phải chứa Cl. Khối lượng Cl trong 7,175 g AgCl :
Đó cũng là khối lượng Cl trong 2,475 g A.
Vậy, khối lượng Cl trong 3,96 g A :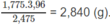
Khối lượng C, H và Cl đúng bằng khối lượng chất A (3,96 g).
Vậy, chất A có dạng C x H y C l z .
x : y : z = 0,08 : 0,16 : 0,08 = 1 : 2 : 1
CTĐGN của A là C H 2 C l .
2. MA = 3,300.30 = 99 (g/mol)
⇒ ( C H 2 C l ) n = 99 ⇒ 49,5n = 99 ⇒ n = 2
CTPT của A là C 2 H 4 C l 2 .
3. Các CTCT