Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
\(n_C=n_{CO_2}=n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,4.1 = 4 (g) < 10,4 (g)
→ A chứa C, H và O.
⇒ mO = 10,4 - 4 = 6,4 (g) ⇒ nO = 0,4 (mol)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,3:0,4:0,4 = 3:4:4
→ CTPT của A có dạng (C3H4O4)n.
Mà: \(n_{A\left(5,2\left(g\right)\right)}=n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\Rightarrow M_A=\dfrac{5,2}{0,05}=104\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{104}{12.3+4+16.4}=1\)
Vậy: CTPT của A là C3H4O4.

Đáp án B
Vì nCO2 = nH2O = 0,03 mol.
⇒ CTTQ của X có dạng CnH2n.
Ta có 0,42 gam X có nX = 0,32÷32 = 0,01 mol.
⇒ MCxH2n = 0,42÷0,01 = 42 ⇒ n = 3

Đáp án B
Vì nCO2 = nH2O = 0,03 mol.
⇒ CTTQ của X có dạng CnH2n.
Ta có 0,42 gam X có nX = 0,32÷32 = 0,01 mol.
⇒ MCxH2n = 0,42÷0,01 = 42 ⇒ n = 3

Gọi công thức phân tử của X là CxHyOz .
Sản phẩm cháy gồm CO2 và H2O.
Ở lần thí nghiệm thứ nhất, bình 1 chứa H2SO4 đậm đặc dư hấp thụ H2O và bình 2 chứa dung dịch nước vôi trong dư hấp thụ CO2.
Ở lần thí nghiệm thứ hai, bình 1 chứa CaO dư hấp thụ CO2 và toàn bộ hơi nước, bình 2 chứa P2O5 dư không hấp thụ gì vì toàn bộ lượng khí đã được hấp thụ ở bình 1. Do đó m2 = 0. Theo định luật bảo toàn khối lượng ta có
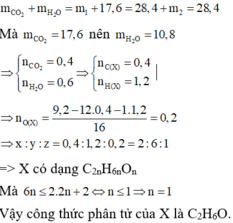

Có 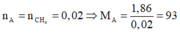
Số mol chất A đem đốt cháy là: x = 0,1 mol
![]()
![]()
0,2 0,2
![]()
0,4 0,2
![]()
0,2 0,2
Suy ra nCO = 0,6(mol).
![]() .
.
Do đó trong phân tử của A có 1 nguyên tử N.
Gọi công thức phân tử của A là CxHyOzN
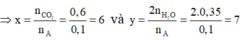
Ta lại có: 6.12 + 7 + 16z + 14 = 93 => z = 0
Vậy chất A có công thức phân tử là C6H7N.
Đáp án D.

\(M_X=\dfrac{1.5}{\dfrac{1.775}{71}}=60\left(g\text{/}mol\right)\)
\(n_X=\dfrac{2.25}{60}=0.0375\left(mol\right)\)
CT : \(C_xH_yO_z\)
\(n_{CaCO_3}=n_{CO_2}=\dfrac{11.25}{100}=0.1125\left(mol\right)\)
\(\Rightarrow n_C=0.1125\left(mol\right)\)
\(m_{bt}=m_{CO_2}+m_{H_2O}=7.65\left(g\right)\)
\(\Rightarrow n_{H_2O}=\dfrac{7.65-0.1125\cdot44}{18}=0.15\left(mol\right)\)
\(\Rightarrow n_H=0.15\cdot2=0.3\left(mol\right)\)
Ta có :
\(x=\dfrac{n_C}{n_X}=\dfrac{0.1125}{0.0375}=3\)
\(y=\dfrac{n_H}{n_X}=\dfrac{0.3}{0.0375}=8\)
\(M=12\cdot3+8+16z=60\left(g\text{/}mol\right)\)
\(\Rightarrow z=1\)
\(CT:C_3H_8O\)

Đáp án A
nCO2=nCaCO3=35/100=0,35 mol
nH2O=3,6/18=0,2 mol
=>mO=mX-mC-mH=5,4 -12.0,35-1.2.0,2=0,8 g
=> nO=0,05 mol
nC:nH:nO=0,35:0,4:0,05=7:8:1
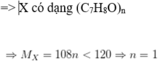
=> CTPT của X là C7H8O
X phản ứng với Na suy ra X có nhóm -OH => Các CTCT của X là
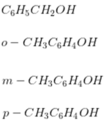

Đáp án B
nX = nO2 (0,32g) = 0,01 (mol) => MX = 42 (g/mol)
mb1 tăng = mH2O = 0,54 (g) => nH2O = 0,03 (mol)
mb2 tăng = mCO2 = 1,32 (g) => nCO2 = 0,03 (mol)
Gọi CTPT X: CxHy
=> x = nCO2/ nX = 3
y = 2nH2O/nX = 6
=> CTPT X: C3H6

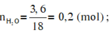
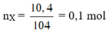
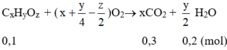

Đáp án C
Vì sản phẩm sau phản ứng gồm H2O (hấp thụ bởi bình 1) và CO2 (hấp thụ bởi bình 2) nên X chứa C, H và có thể có O. Gọi công thức phân tử của X là CxHyOz.
Vì hóa hơi hoàn toàn 5,2 gam X thu được thể tích bằng với thể tích của 1,6 gam O2 trong cùng điều kiện
Vậy X là C3H4O4.