Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nC2H2 = 1/26 (mol)
Đốt cháy 1/26 mol C2H2 tỏa ra 49,98 kJ
=> Đốt cháy 1 mol C2H2 tỏa ra x kJ
=> x = 1 x 49,98 : (1/26) = 1299,48 kJ
=> ${\Delta _r}H_{298}^0$ = -1299,48 kJ (vì đây là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm)

\(C_2H_6+\dfrac{7}{2}O_2->2CO_2+3H_2O\\ \Delta_rH^o_{298}=2\left(-393,5\right)+3\left(-285,8\right)-\left(-84,7\right)\\ \Delta_rH^o_{298}=-1559,7kJ\)
Phương trình nhiệt hoá học thì không cần ghi điều kiện nhé.

a)
$C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O$
$2C_2H_2 + 5O_2 \xrightarrow{t^o} 4CO_2 + 2H_2O$
$C_2H_4 + Br_2 \to C_2H_4Br_2$
$C_2H_2 + 2Br_2 \to C_2H_2Br_4$
b)
n C2H4 = a(mol) ; n C2H2 = b(mol)
=> 28a + 26b = 2,96(1)
Mặt khác :
n B = 1,232/22,4 = 0,055(mol)
n Br2 = 13,6/160 = 0,085(mol)
Suy ra :
(a + b) / ( a + 2b) = 0,055/0,085 (2)
Từ (1)(2) suy ra a = 0,05 ; b = 0,06
Theo PTHH :
n CO2 = 2a + 2b = 0,22(mol) => m1 = 0,22.44 = 9,68(gam)
n CO2 = 2a + b = 0,16(mol) => m2 = 0,16.18 = 2,88(gam)

Chọn A
Cách 1:
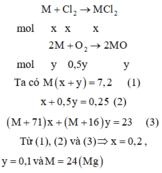
Cách 2:
Gọi số mol của Cl2 và O2 phản ứng lần lượt là x và y mol
→ nkhí = 0,25 mol → x + y = 0,25 (1)
Bảo toàn khối lượng có mkhí= 23 – 7,2= 15,8 gam
→ 71x + 32y = 15,8 (2)
Từ (1) và (2) → x = 0,2 và y = 0,05
Bảo toàn electron có:
2.nM = 2.nCl2 + 4.nO2 → nM= 0,3 → MM = 7,2 : 0,3 = 24 (g/mol)
Vậy kim loại M là Mg.

Đáp án A
mrắn sau − mM = mX ⇒ 71nCl2 + 32nO2 = 23 − 7,2 = 15,8 g (1)
⇒nkhí = nCl2 +nO2 = 0,25 mol (2)
Giải hệ (1) và (2) ⇒nCl2 = 0,2; nO2 = 0,05 mol
Gọi hóa trị của M là x
Bảo toàn e

M = ![]() = 12x, x = 2 => M = 24 (Mg)
= 12x, x = 2 => M = 24 (Mg)
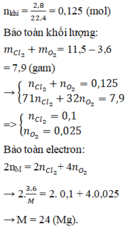

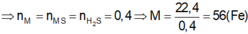
\(\Delta_rH=-\dfrac{50,01kJ}{\dfrac{1}{26}mol}=-1300,26kJ\cdot mol^{-1}\)
Mặt khác, khi đốt 1 mol methane chỉ toả ra lượng nhiệt khoảng 890,2 kJ, thấp hơn nhiều so với acetylene nên acetylene được dùng trong đèn xì.