Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Thứ tự các phản ứng điện phân xảy ra:
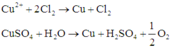
Do đó kim loại bám vào catot là Cu, khí thoát ra ở anot là Cl2, có thể có O2.
![]()
Áp dụng định luật bảo toàn mol electron, ta có:
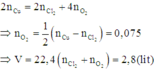

Đáp án C
Ở t giây ta thu được ở anot 0,12 mol hỗn hợp khí gồm Cl2 và O2.
Ở 2t giây ta thu được thể tích khí ở anot gấp 3 lần ở catot.
Goi số mol Cl2 và O2 ở t giây lần lượt là a, b => a + b = 0,12
Bảo toàn e: n e = 2a + 4b
Lúc 2t giây: n e = 4a + 8b
Lúc này ở anot thu được Cl2 a mol và O2
Do vậy ở catot thu được là H2 với số mol H2
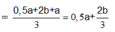
Bảo toàn e: n C u 2 +
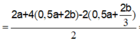
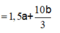
![]()
Giải hệ: a = b = 0,06 mol
Do vậy số mol KCl là 0,12 mol và CuSO4 là 0,29 mol.
m = 55,54 gam.

Đáp án B
Cu2+:x
Cl-: y
Ở catot thoát ra khí => H2O bị đp
Catot:
Cu2+ +2e → Cu
x 2x
H2O +1e → 0,5H2 + OH-
y-2x 0,5y-x
Anot:
Cl- - 1e → 0,5Cl2
y y 0,5y
=> 0,5y = 4(y-2x) => x/y=3/8
=>%mCuSO4 = 160.3/(160.3+74,5.8) = 44,61%

Đáp án B
Cu2+:x
Cl-: y
Ở catot thoát ra khí => H2O bị đp
Catot:
Cu2+ +2e → Cu
x 2x
H2O +1e → 0,5H2 + OH-
y-2x 0,5y-x
Anot:
Cl- - 1e → 0,5Cl2
y y 0,5y
=> 0,5y = 4(y-2x) => x/y=3/8
=>%mCuSO4 = 160.3/(160.3+74,5.8) = 44,61%


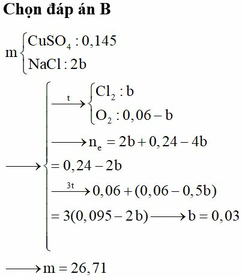



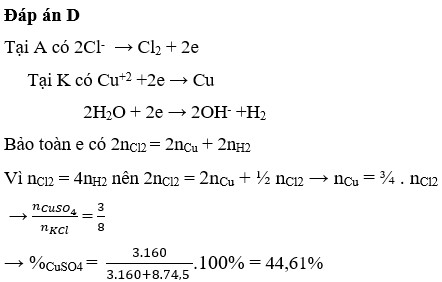
Đáp án C
Trong dung dịch ban đầu có 0,4 mol Fe 3 + , 0,2 mol Cu 2 + , 0,4 mol Cl - và các ion khác không tham gia phản ứng điện phân
- Khi catot tăng 12,8 gam, tức là Cu2+ vừa hết, phản ứng (2) vừa kết thúc. Khi đó dung dịch chỉ có màu trắng xanh của Fe2+ nên phương án A sai
- Khi khối lượng catot tăng lên 6,4 gam, tức là đã có 0,1 mol Cu2+ bị điện phân. Vậy phản ứng (1) đã xảy ra hết, phản ứng (2) xảy ra một phần
Áp dụng công thức : q = ∑ n i z i F
Trong đó ni là số mol chất i (phân tử hoặc ion) bị điện phân, zi là số e của chất i trao đổi ở điện cực
Ta có: q = (0,4.1 + 0,1.2).96500= 57900 (C)
Phương án B sai
- Khi có 4,48 lít khí thoát ra ở anot, tức là có 0,2 mol khí thoát ra suy ra phản ứng (a) xảy ra hoàn toàn và vừa đủ. Tại anot có 0,4 mol e trao đổi
Đông thời tại catot phản ứng (1) xảy ra hoàn toàn và vừa đủ. Chưa có kim loại kết tủa trên điện cực. Phương án C đúng
- Khi có khí bắt đầu thoát ra ở catot tức là các phản ứng (1) (2) (3 ) (4) đã xảy ra hoàn toàn. Số e trao đổi ở catot là 1,4 mol.
Tại anot, phản ứng (a) đã xảy ra hoàn toàn và có 0,4 mol e đã tiêu thụ trong phản ứng (a), sinh ra 0,2 mol Clo
Số e tiêu thụ cho phản ứng (b) sẽ là 1 mol. Vậy có 0,25 mol khí oxi sinh ra.
Tổng số mol khí sinh ra tại anot trong trường hợp này là 10,08 lít. Phương án D sai