Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : C
KClO3 -----------> KCl + 3/2O2 (1)
Ca(ClO2)2 ---------> CaCl2 + 2O2
Ca(ClO3)2 ----------> CaCl2 + 3O2
CaCl2 -----------> CaCl2
KCl ---------------> KCl chất rắn B là KCl và CaCl2
ta có n O 2 = 0 , 78 m o l
bảo toàn khối lượng ta có
mA = mB + mO2 => mB = 58,72 g
CaCl2 + K2CO3 -----------> CaCO3 + 2KCl
0,18____0,18__________________0,36
xét hỗn hợp B ta có
m K C l = m B - m C a C l 2 = 38 , 74 g
vậy khối lượng KCl ở D là mKCl = 38,74 + 0,36.74,5 = 65,56
khối lượng KCl tại A = 3 /22.(Lượng KCl trong dung dịch D )
m KCl tại A = 8,94g
vậy khối lượng KCl tại phản ứng 1 là 38,74 – 8,94 = 29,8 g
theo phản ứng 1 thì m K C l O 3 = 49 g
=>% = 58,55 %

Đáp án B
► Giả sử KOH không dư ||⇒ nKNO2 = nKOH = 0,5 mol ⇒ mrắn ≥ mKNO2 = 42,5(g)
⇒ vô lí!. ⇒ KOH dư. Đặt nKNO3 = x; nKOH dư = y. Bảo toàn nguyên tố Kali: x + y = 0,5.
Rắn gồm KNO2 và KOH dư ⇒ 85x + 56y = 41,05 ||⇒ giải hệ có: x = 0,45 mol; y = 0,05 mol.
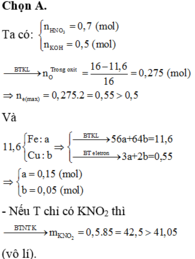
● Đặt nFe = a; nCu = b ⇒ mA = 56a + 64b = 11,6(g) || 16(g) rắn gồm Fe2O3 và CuO.
⇒ 160.0,5a + 80b = 16 ||⇒ giải hệ có: a = 0,15 mol; b = 0,05 mol.
nHNO3 = 0,7 mol; nNO3–/X = nKNO3 = 0,45 mol. Bảo toàn nguyên tố Nitơ: nN/B = 0,25 mol.
Bảo toàn nguyên tố Hidro: nH2O = 0,35 mol. Bảo toàn nguyên tố Oxi: nO/B = 0,4 mol.
||⇒ Bảo toàn khối lượng: mX = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2(g).
► nNO3–/X < 3nFe + 2nCu ⇒ X gồm muối Fe(NO3)2, Fe(NO3)3 và Cu(NO3)2.
Giải hệ có: nFe(NO3)3 = 0,05 mol ||⇒ C%Fe(NO3)3 = 0,05 × 242 ÷ 89,2 × 100% = 13,56%

Đáp án : D
Ta có : nKOH = 0,5 (mol)
Ta nhận xét nhanh như sau :
Nếu KOH thiếu thì Z sẽ là KNO3 và các muối của kim loại
(bảo toàn nguyên tố K)
→ m chất rắn
→ m K N O 2 = 0,5.(39 + 46) = 41,5 (vô lý).
(bảo toàn nguyên tố K)
→ 41 , 05 K N O 2 : 0 , 45 K O H : 0 , 05
(bảo toàn khối lượng)
→ nO trong oxit = 0,275 → B T e ne = 0,55 (mol)
→ 11 , 6 F e : 0 , 15 m o l C u : 0 , 05 m o l
Và n H N O 3 =0,7(mol) → B T N T . H = n H 2 O sin h r a = 0,35 (mol)
Vậy trong X có :
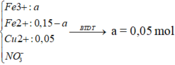
→ B T K L 11,6 + 0,7.63 = 11,6 + 0,45.62 + mB + 0,35.18
→ mB = 9,9 gam
→ %mFe(NO3)3 = 13,56%

Đáp án : B
Vì kim loại tan hết nên HNO3 dư
Khi X + KOH => thu được kết tủa
+) Giả sử KOH dư => chất rắn 16,0g gồm Fe2O3 ; CuO (*)
Khi đó T gồm KNO3 và KOH => Nung lên thành KNO2 và KOH với số mol lần lượt là x và y
=> 41,05 = 85x + 56y
Và nK = 0,5 = x + y
=> x = 0,45 mol ; y = 0,05 mol
Gọi số mol Fe và Cu trong A lần lượt là a và b mol
=> 56a + 64b = 11,6g
Và 80a + 80b = 16g (*)
=> a = 0,15 mol ; b = 0,05 mol
+) Nếu chỉ có Fe3+ và Cu2+ => nKOH < 3nFe + 2nCu ( Vô lí )
=> Trong X có Fe2+ : u mol và Fe3+ : v mol
=> HNO3 phải hết
=> u + v = 0 , 15 2 u + 3 v = 0 , 45 => u = 0 , 1 v = 0 , 05
Có nFe(NO3)3 = 0,05 mol
Ta thấy mN2 < mB < mNO2
=> 0,35.28 < mB < 46.0,7
=> 9,8 < mB < 32,2g
BTKL : 66,9g < mdd sau < 89,3g
=> 13,55% < %mFe(NO3)3 < 18,09%
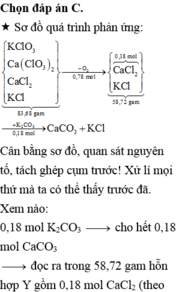

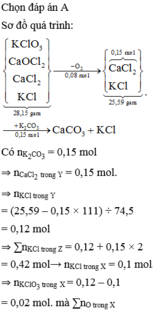
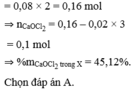
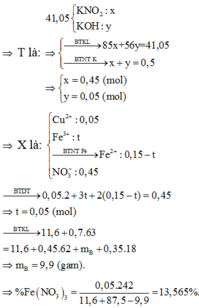



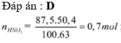
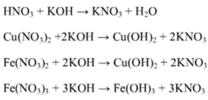
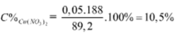
Chọn đáp án C
Ta có