Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. Các kim loại và gốc không được ở cạnh nhau:
\(Ba\) và sunfat,\(Ba\) và cacbonat,\(Mg\) và cacbonat,\(Pb\) và clorua,\(Pb\) và sunfat,\(Pb\) và cabonat
Vậy mỗi ống chứa các dd; \(K_2CO_3,Pb\left(NO_3\right)_2,MgSO_4,BaCl_2\)
b.
Nhỏ dd \(HCl\) vào các ống (thí nghiệm thực hiện ở nhiệt độ thấp)
- \(K_2CO_3 \) có khí không màu
- \(Pb\left(NO_3\right)_2\) có kết tủa trắng
\(K_2CO3+2HCl->2KCl+CO_2+H_2O\)
\(Pb\left(NO_3\right)_2+2HCl->PbCl_2+2HNO_3\)
Nhỏ \(NaOH\) vào 2 dung dịch còn lại
- \(MgSO_4\) kết tủa trắng
- Còn lại là \(BaCl_2\)
\(MgSO_4+2NaOH->Mg\left(OH\right)_2+Na_2SO_4\)
Tham khảo nhé !

a,
Các kim loại và gốc không được ở cạnh nhau: BaBa và sunfat, BaBa và cacbonat, Mg và cacbonat, Pb và clorua, Pb và sunfat, Pb và cacbonat.
Vậy mỗi ống chứa các dd: K2CO3, Pb(NO3)2, MgSO4, BaCl2
b,
Nhỏ dd HCl vào các ống (thí nghiệm thực hiện ở nhiệt độ thấp).
- K2CO3 có khí không màu.
- Pb(NO3)2 có kết tủa trắng.
K2CO3+2HCl→2KCl+CO2+H2O
Pb(NO3)2+2HCl→PbCl2+2HNO3
Nhỏ NaOH vào 2 dung dịch còn lại.
- MgSO4 kết tủa trắng.
- Còn lại là BaCl2
MgSO4+2NaOH→Mg(OH)2+Na2SO4

a) Ta có các ống nghiệm sau: K2CO3, Pb(NO3)2, MgSO4, BaCl2.
Giải thích. Lọ K2CO3 là phải có vì gốc CO3 2- kết hợp với các gốc kim loại Ba, Mg, Pb đều tạo kết tủa không tạo dung dịch.
b) Phân biệt:
Cho HCl vào 4 dung dịch: K2CO3, Pb(NO3)2, MgSO4, BaCl2.
-> Tạo khí: K2CO3:
K2CO3 + 2HCl -> 2KCl + H2O + CO2↑
-> Không hiện tượng: Pb(NO3)2, MgSO4, BaCl2. ------------nhóm A.
Cho dd NaCl vào nhóm A:
+ Tạo kết tủa: Pb(NO3)2:
2NaCl + Pb(NO3)2 -> PbCl2↓ + 2NaNO3
+ Không hiện tượng: MgSO4, BaCl2------------nhóm B.
Cho tiếp dd Na2SO4 vào nhóm B:
-> Tạo kết tủa: BaCl2:
Na2SO4 + BaCl2 -> BaSO4↓ + 2NaCl
-> Không hiện tượng: MgSO4.
@Cẩm Vân Nguyễn Thị

a) Ta có các ống nghiệm sau: K2CO3, AgNO3, MgSO4, BaCl2.
Giải thích. Lọ K2CO3 là phải có vì gốc CO3 2- kết hợp với các gốc kim loại Ba, Mg, Ag đều tạo kết tủa không tạo dung dịch.
b) Phân biệt:
Cho HCl vào 4 dung dịch: K2CO3,AgNO3, MgSO4, BaCl2.
-> Tạo khí: K2CO3:
K2CO3 + 2HCl -> 2KCl + H2O + CO2↑
-> Không hiện tượng: AgNO3, MgSO4, BaCl2. ------------nhóm A.
Cho dd NaCl vào nhóm A:
+ Tạo kết tủa: AgNO3:
NaCl + AgNO3-> AgCl2↓ + NaNO3
+ Không hiện tượng: MgSO4, BaCl2------------nhóm B.
Cho tiếp dd Na2SO4 vào nhóm B:
-> Tạo kết tủa: BaCl2:
Na2SO4 +BaCl2 -> BaSO4↓ + 2NaCl
-> Không hiện tượng: MgSO4.
a. Các dd lần lượt là BaCl2; MgSO4; AgNO3;K2CO3
b. Trích mẫu thử, cho dd HCl vào các mẫu thử
+ Xuất hiện bọt khí: K2CO3
+ Kết tủa: AgNO3
+ Không ht: BaCl2 và MgSO4
- Tiếp tục cho dd Ba(NO3)2 vào nhóm không ht
+ Kết tủa: MgSO4
+ Không ht: BaCl2
\(PTHH:K_2CO_3+2HCl\rightarrow2KCl+H_2O+CO_2\)
\(AgNO_3+HCl\rightarrow AgCl+HNO_3\)
\(MgSO_4+Ba\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+BaSO_4\)

chỗ kia là không trùng kim loại lẫn gốc axit chứ không phải là dùng
a) Ta có các ống nghiệm sau: K2CO3, Pb(NO3)2, MgSO4, BaCl2.
Giải thích. Lọ K2CO3 là phải có vì gốc CO3 2- kết hợp với các gốc kim loại Ba, Mg, Pb đều tạo kết tủa không tạo dung dịch.
b) Phân biệt:
Cho HCl vào 4 dung dịch: K2CO3, Pb(NO3)2, MgSO4, BaCl2.
-> Tạo khí: K2CO3:
K2CO3 + 2HCl -> 2KCl + H2O + CO2↑
-> Không hiện tượng: Pb(NO3)2, MgSO4, BaCl2. ------------nhóm A.
Cho dd NaCl vào nhóm A:
+ Tạo kết tủa: Pb(NO3)2:
2NaCl + Pb(NO3)2 -> PbCl2↓ + 2NaNO3
+ Không hiện tượng: MgSO4, BaCl2------------nhóm B.
Cho tiếp dd Na2SO4 vào nhóm B:
-> Tạo kết tủa: BaCl2:
Na2SO4 + BaCl2 -> BaSO4↓ + 2NaCl
-> Không hiện tượng: MgSO4.

Ta có các ống nghiệm sau: K2CO3, Pb(NO3)2, MgSO4, BaCl2.
Giải thích. Lọ K2CO3 là phải có vì gốc CO3 2- kết hợp với các gốc kim loại Ba, Mg, Pb đều tạo kết tủa không tạo dung dịch.
Phân biệt:
Cho HCl vào 4 dung dịch: K2CO3, Pb(NO3)2, MgSO4, BaCl2.
-> Tạo khí: K2CO3:
K2CO3 + 2HCl -> 2KCl + H2O + CO2↑
-> Không hiện tượng: Pb(NO3)2, MgSO4, BaCl2. ------------nhóm A.
Cho dd NaCl vào nhóm A:
+ Tạo kết tủa: Pb(NO3)2:
2NaCl + Pb(NO3)2 -> PbCl2↓ + 2NaNO3
+ Không hiện tượng: MgSO4, BaCl2------------nhóm B.
Cho tiếp dd Na2SO4 vào nhóm B:
-> Tạo kết tủa: BaCl2:
Na2SO4 + BaCl2 -> BaSO4↓ + 2NaCl
-> Không hiện tượng: MgSO4.

a)
- Vì Ba, Mg, Pb đều kết tủa với CO3 nên muối tan CO3 là :K2CO3
- Vì Ba và Pb đều kết tủa với SO4 nên muối tan SO4 là: MgSO4
- Vì Pb kết tủa với Cl nên muối tan Cl là: BaCl2
- Còn lại muối kia là: Pb(NO3)2
b) -Dùng HCl cho vào:
+ có khí bay lên là K2CO3: K2CO3+2HCl\(\rightarrow\)2KCl+CO2+H2O
+ Có kết tủa trắng là Pb(NO3)2: Pb(NO3)2+2HCl\(\rightarrow\)PbCl2+2HNO3
+ Không hiện tượng là BaCl2 và MgSO4
- Cho H2SO4 vào 2 mẫu còn lại:
+có kết tủa trắng là BaCl2: BaCl2+H2SO4\(\rightarrow\)BaSO4+2HCl
+ không hiện tượng là MgSO4

câu 2
nhận xét thấy:
Ba có 2 gốc a xit kết hợp tạo dung dịch: Cl và NO3
Pb:có 1 gốc a xit kết hợp tạo dung dịch: NO3
Mg :có 3 gốc a xit kết hợp tạo dung dịch: SO4,Cl và NO3
K kết hợp được cả 4 gốc
vậy các ống đựng: BaCl2;PbNO3;MgSO4;K2CO3
nhận biết:
trích mẫu thử
cho các mẫu thử vào HCl
nếu có kêt tủa-> PbNO3
nếu có khí => K2CO3
không phản ứng : BaCL2;MgSO4
cho 2 dung dịch còn lại vào H2SO4 nếu có kết tủa => BaCL2
còn lại MgSO4
pthh tự viết

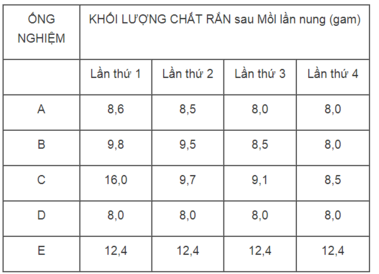
1. Ống nghiệm E (khối lượng CuCO 3 không thay đổi).
2. Ống nghiệm C, vì khác với các kết quả của những ống nghiệm A, B, D.
3. Sau lần nụng thứ 3 thì toàn lượng CuCO 3 đã bị phân huỷ hết thành CuO.
4. Ống nghiệm D.
a) Ta có các ống nghiệm sau: K2CO3, Pb(NO3)2, MgSO4, BaCl2.
Giải thích. Lọ K2CO3 là phải có vì gốc CO3 2- kết hợp với các gốc kim loại Ba, Mg, Pb đều tạo kết tủa không tạo dung dịch.
b) Phân biệt:
Cho HCl vào 4 dung dịch: K2CO3, Pb(NO3)2, MgSO4, BaCl2.
-> Tạo khí: K2CO3:
K2CO3 + 2HCl -> 2KCl + H2O + CO2↑
-> Không hiện tượng: Pb(NO3)2, MgSO4, BaCl2. ------------nhóm A.
Cho dd NaCl vào nhóm A:
+ Tạo kết tủa: Pb(NO3)2:
2NaCl + Pb(NO3)2 -> PbCl2↓ + 2NaNO3
+ Không hiện tượng: MgSO4, BaCl2------------nhóm B.
Cho tiếp dd Na2SO4 vào nhóm B:
-> Tạo kết tủa: BaCl2:
Na2SO4 + BaCl2 -> BaSO4↓ + 2NaCl
-> Không hiện tượng: MgSO4.