Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Vì Al(OH)3 là 1 hyđroxit lưỡng tính
⇒ có thể tác dụng với axit và bazo.
Cho X vào HCl mà tạo khí thì trong X chắc chắn có Al (do Cu và Ag không phản ứng với HCl).
Do có Al nên Cu2+ và Ag+ phản ứng hết.
Số mol Al ban đầu:
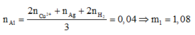
![]()

Đáp án D
Đặt số mol C, S lần lượt là x, y
12 x + 32 y = 3 , 68 m ↓ = m BaCO 3 + m BaSO 3 = 197 x + 217 y = 38 , 83 g ⇒ x = 0 , 12 y = 0 , 07 Quy đổi : C , S → X : M X = 3 , 68 0 , 12 + 0 , 07 = 368 19 NaOH , KOH → ROH
0,19 mol X + 0,1a mol ROH ® m1 gam muối/V1 ml dung dịch Z
0,19 mol X + 0,16a mol ROH ®m2 gam muối/V2 ml dung dịch T
6V1 ml Z + V2 ml T ® muối trung hòa
Þ Chứng tỏ Z chứa muối axit, T chứa kiềm dư và 6 n HXO 3 - ( Z ) = n OH - ( T )

=> b.(0,38-0,1a)=0,16a-0,38 => a=3,5
m 2 - m 1 = m ROH ( T ) + m RXO 3 ( T ) - m RXO 3 ( Z ) - m RHXO 3 ( Z ) m 2 - m 1 = ( R + 17 ) . 0 , 18 + 2 R + 1280 19 . 0 , 19 - 0 , 16 - R + 1299 19 . 0 , 03 = 8 , 82 ⇒ R = 193 7 ⇒ m 1 = 193 7 + 17 . 0 , 18 + 2 . 193 7 + 1280 19 . 0 , 19 = 31 , 3 g m 2 = 2 . 193 7 + 1280 19 . 0 , 16 + 193 7 + 1299 19 . 0 , 03 = 22 , 48 g ⇒ m 1 + m 2 = 53 , 78 gần nhất với giá trị 54 .

Đáp án B
Chọn số mol mỗi chất là 1 mol
A. Loại vì m 1 < m 2 < m 3
m 1 = + = 1.100 + 1.90 = 190 (g)
m 2 = + = 1.100 + 1.116 = 216 (g)
m 3 = mAgCl + mAg = 2.143,5 + 1.108 = 395 (g)
B. Chọn vì m 1 < m 3 < m 2
m 1 = = 90 (g) ; m 2 = = 116 (g) ; m 3 = mAg = 108 (g)
C. Loại vì m 3 > m 2 > m 1
m 1 = = 90 (g); m 2 = = 116 (g) ; m 3 = mAgCl + mAg = 3.143,5 + 1.108 = 538,5 (g)
D. Loại vì m 1 = m 2 > m 3
m 1 = = 197 (g); m 2 = = 197 (g); m 3 = mAgCl = 143,5 (g)

Chọn đáp án C
♦ giải đốt a mol X + O2
b mol CO2 + c mol H2O.
b – c = 4a ⇒ tương quan đốt: ∑nCO2 – ∑nH2O = (5 – 1).nX ||⇒ X có 5π.
trieste sẵn có 3πC=O ⇒ còn 2πC=C nữa ||⇒ X + 2H2 → Y.
có nX = ½.nH2 = 0,08 mol; mX = mY – mH2 = 20,48 gam.
♦ 20,48 gam X + 0,3 mol NaOH (có dư) → m2 gam c.rắn + 0,08 mol C3H5(OH)3.
||⇒ BTKL có m2 = 20,48 + 0,3 × 40 – 0,08 × 92 = 25,12 gam.

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư ⇒ C u 2 + hết
Giả sử chỉ có Mg phản ứng ![]()
=> tăng giảm khối lượng ![]()
=> vô lý => Fe phản ứng
Bảo toàn khối lượng gốc kim loại:
24x + 56y = 9,2 + 0,13.64 - 12,48 => x = 0,07 mol; y = 0,06 mol
=> rắn gồm 0,07 mol MgO và 0,03 mol F e 2 O 3 => m = 7,6 (g)

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư => C u 2 + hết
Giả sử chỉ có Mg phản ứng

Bảo toàn khối lượng gốc kim loại:
![]()
![]()
=> rắn gồm 0,07 mol MgO và 0,03 mol
![]()

Đáp án C
Do X tác dụng với HCl sinh ra khí nên Al dư, CuSO4 và AgNO3 hết
nAl dư=nH2/1,5=0,02 mol
nCu=nCuSO4=0,03 mol
nAg=nAgNO3=0,03 mol
BT e: 3nAl pư=2nCu+nAg=> nAg pư=(0,03.2+0,03)/3=0,03 mol
m1=(0,03+0,02).27=1,35 gam
m2=0,03.64+0,03.108+0,02.27=5,7 gam