Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
Theo bản chất “Lòng tham vô đáy” khi cho các kim loại vào dung dịch muối.Các kim loại mạnh nhất sẽ cướp anion trước,sau đó mới tới các kim loại yếu hơn.
Dễ thấy
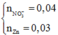
do đó dung dịch cuối cùng có nZn(NO3)2=0,02(mol)
![]()
->m=1,6(g)

Đáp án C
Ta có: ![]()
Ta có: ![]()
Bảo toàn điện tích:
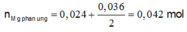
Do vậy rắn Z chứa 0,038 mol Mg dư.
BTKL: m = 4,826 - 0,038.24 + 4,21 - 0,036.108 - 0,024.64 = 2,7 gam

Đáp án A
Các phản ứng đều là kim loại đẩy kim loại ra khỏi dung dịch muối → anion được bảo toàn.
Thứ tự các kim loại trong dãy điện hóa: Zn > Fe > Cu > Ag.
Theo đó, dung dịch cuối cùng chỉ chứa một muối duy nhất là 0,02 mol Zn(NO3)2.
ó Phản ứng: 5,2 gam Zn + ? gam Y → 0,02 mol Zn(NO3)2 + 5,82 gam chất rắn Z.
→
bảo toàn khối lượng ta có ![]()
ó Phản ứng: m gam (Cu, Fe) + 0,04 mol AgNO3 → 4,4 gam Y + 4,16 gam chất rắn X.
→ bảo toàn khối lượng ta có m = 4,4 + 4,16 – 0,04´170 = 1,76 gam.

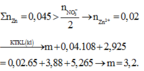
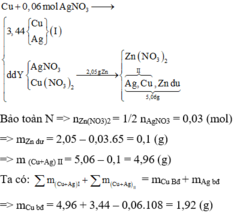

Chọn đáp án D
● Giả sử Zn hết ⇒ Z chứa muối Zn(NO3)2 ⇒ cần 0,045 × 2 = 0,09 mol NO3–.
⇒ vô lí ⇒ Zn dư ⇒ Z chỉ chứa muối Zn(NO3)2 ⇒ nZn(NO3)2 = 0,04 ÷ 2 = 0,02 mol.
Do NO3– được bảo toàn nên ta chỉ cần bảo toàn khối lượng gốc kim loại.
► m = 3,217 + 0,02 × 65 + 3,88 – 0,045 × 65 – 0,04 × 108 = 1,152(g) ⇒ chọn D