Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

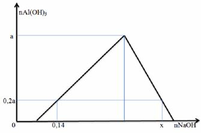
Vì nAl(OH)3 max = a → nAlCl3 = a
Giả sử số mol của AlCl3 và HCl trong mỗi phần là a, b
Bảo toàn Cl: 3a + b = 0,5 (1)
HCl + NaOH → NaCl + H2O
b → b
– Tại nNaOH = 0,14: kết tủa đang lên max (chưa bị hòa tan)
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
0,6a ← 0,2a
=> b + 0,6a = 0,14 (2)
Từ (1) và (2) => a = 0,15 và b = 0,05
– Tại nNaOH = x: kết tủa bị hòa tan một phần
Al(OH)3 + NaOH → NaAlO2 + 2H2O
0,12 → 0,12
Dư: 0,03
→ x = 0,05 + 3.0,15 + 0,12 = 0,62 (mol)
Vậy x = 0,62

a)X gồm Fe,Ag
\(Fe + 2AgNO_3 \to Fe(NO_3)_2 + Ag(1)\\ Fe + 2HCl \to FeCl_2 + H_2(2)\\ 2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(3)\\ 2Ag + 2H_2SO_4 \to Ag_2SO_4 + SO_2 + 2H_2O(4)\\\)
b) Phần 1,gọi n\(n_{Ag} = a(mol)\)
Theo PTHH (2) : \(n_{Fe} = n_{H_2} = 0,1(mol)\)
Suy ra : m2 = 0,1.56 + 108a = 5,6 + 108a(gam)
Phần 2, \(n_{Ag} = ak(mol) ; n_{Fe} = 0,1k(mol)\)
Theo PTHH (3)(4) : \(n_{SO_2} = \)0,5.ak + 0,1k.1,5 = 0,5ak + 0,15k = 0,4
⇒ k(0,5a + 0,15) = 0,4(1)
m3 = 108.ak + 0,1k.56 (gam)
Ta có :
\(m_3 - m_2 = 16,4 \Rightarrow m_3 = 16,4 + m_2\)
⇔ k(108a + 5,6) = 16,4 + 5,6 + 108a = 22+ 108a(2)
Ta lấy (1) : (2), ta có :
\(\dfrac{0,5a + 0,15}{108a + 5,6} = \dfrac{0,4}{22 + 108a}\)⇒ a = 0,1
Vậy : k = \(\dfrac{0,4}{0,5a + 0,15} = 2\)
Vậy X gồm :
Fe : 0,1 + 0,1.2 = 0,3(mol)
Ag : 0,1 + 0,1.2 = 0,3(mol)
Fe + 2AgNO3 →Fe(NO3)2 + 2Ag
0,3.....0,3...............................0,3.........(mol)
Vậy :
m = (0,3 + 0,3).56 = 33,6 gam
V = \(\dfrac{0,3}{1}\) = 0,3(lít)
phần tính a bạn giải chi tiết dùm mình dc không, mình giải ko ra

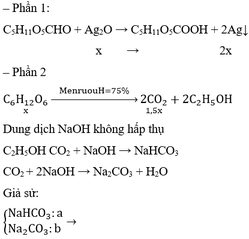
mdd giảm = m↓ - mCO2 → mCO2 = 10 - 3,4 = 6,6 gam → nCO2 = 6,6 : 44 = 0,15 mol.
C6H12O6 enzim−−−−→30−35oC→30-35oCenzim2C2H5OH + 2CO2
Theo phương trình: nC6H12O6 = 0,15 : 2 = 0,075 mol.
Mà H = 90% → nC6H12O6 = 0,075 : 90% = 1/12 mol → m = 180 x 1/12 = 15 gam

Đặt số mol Fe3O4 là x (mol)
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
x..............8x..........2x............x
Cu + 2FeCl3 ⟶ 2FeCl2 + CuCl2
x.........2x................2x.............x
Kim loại không tan là Cu
Dung dịch Y gồm FeCl2, CuCl2 và HCl dư
=> \(n_{FeCl_2}=x+2x=3x\left(mol\right);n_{CuCl_2}=x\left(mol\right)\)
\(n_{OH^-}=0,5.1+0,5.1=1\left(mol\right)\)
\(H^+_{\left(dư\right)}+OH^-\rightarrow H_2O\)
\(Fe^{2+}+2OH^-\rightarrow Fe\left(OH\right)_2\)
3x..........6x...............3x
\(Cu^{2+}+2OH^-\rightarrow Cu\left(OH\right)_2\)
x.............2x.................x
Kết tủa là Cu(OH)2 và Fe(OH)2
Ta có : \(3x.90+x.98=36,8\)
=> x=0,1 (mol)
=> \(m_{Cu}=x.64+1,6=8\left(g\right)\)
=> \(m=0,1.232+8=31,2\left(g\right)\)
Mặt khác : \(n_{HCl\left(dư\right)}=1-\left(6x+2x\right)=0,2\left(mol\right)\)
=> \(n_{HCl\left(bđ\right)}=8x+0,2=1\left(mol\right)\)









Tính toán theo PTHH :
Fe3O4 + 8 HCl → 2 FeCl3 + FeCl2 + 4 H2O
FeCl2 + ½ Cl2 → FeCl3
FeCl2 + 3 AgNO3 → 2 AgCl + Ag + Fe(NO3)3
FeCl3 + 3 AgNO3 → 3 AgCl + Fe(NO3)3
Bảo toàn khối lượng
m2 – 0,5 m1 = m Cl2 ( lưu ý hỗn hợp chia làm 2 phần nên muối phản ứng ở mỗi phần là 0,5 m1 )
m2 – 0,5 m1 = m Cl2 => m Cl2 = 1,42 => n Cl2 = 0,02 mol
Theo PTHH : n FeCl2 = n Cl2 . 2 = 0,04 mol
Theo PTHH : n FeCl2 . 2 = n FeCl3 = 0,08 mol
Theo PTHH : n AgCl = 2 . nFeCl2 + 3 . n FeCl3 = 0,08 .3 + 0,04 .2 = 0,32 mol
n Ag = n FeCl2 = 0,04 mol
=> m Chất rắn = m Ag + m AgCl = 0,04 . 108 + 0,32 . 143,5 = 50,24 g
phản ứng của Fe2+ + Ag+ → Fe+3 + Ag