Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
hhX gồm axetilen và etan (tỉ lệ mol 1 : 3) qua xt, to
→ hhY gồm CH3-CH3, CH2=CH2, CH≡CH và H2, dY/H2 = 58/7.
Giả sử có 1 mol CH≡CH và 3 mol H2 ban đầu.
Theo BTKL: mY = mX = 1 x 26 + 3 x 30 = 116 gam
→ nY = 116 : (58/7 x 2) = 7 mol.
nH2 = nY - nX = 7 - 4 = 3 mol.
nliên kết π trong 7 mol Y = 2 x nCH≡CH + nH2 = 5.
nBr2 = nliên kết π trong 0,7 mol Y = 0,5 mol

\(\left\{{}\begin{matrix}n_{C_nH_{2n-2}}+n_{H_2}=\dfrac{8,96}{22,4}=0,4\\n_{C_nH_{2n-2}}=n_{H_2}\end{matrix}\right.\)
=> \(n_{C_nH_{2n-2}}=n_{H_2}=0,2\left(mol\right)\)
\(n_{H_2\left(pư\right)}=0,4-\dfrac{6,72}{22,4}=0,1\left(mol\right)\)
Bảo toàn liên kết: \(2.n_{C_nH_{2n-2}}=n_{H_2\left(pư\right)}+n_{Br_2}\)
=> \(n_{Br_2}=0,3\left(mol\right)\)
=> B

Đáp án B
Ta có:
![]()
Gọi a là số mol H2 phản ứng, b là số mol ankin còn dư trong Y.
Ta có: n Z = 0,85 = 1,4 - a -b
Mặt khác cho Z vào dung dịch brom dư thấy có 0,05 mol Br2 suy ra n π ( Z ) = 0 , 05 m o l
Bảo toàn liên kết π: 0,2.2 + 0,1.2 + 0,15 - a - 2b = 0,05
Giải hệ: a=0,4; b=0,15.
→ n Y = 1,4 - 0,4 = 1 mol
Ta có: m Y = m X = 19 , 5 g a m
![]()

Đáp án B
Sơ đồ ta có
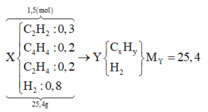
+ Theo định luật bảo toàn khối lượng ta có mX = mY = 25,4 gam.
⇒ nY = 25,4÷25,4 = 1 mol ⇒ nHỗn hợp giảm 0,5 mol ⇒ nH2 đã pứ = 0,5 mol.
Với ∑nπC=C = 0,3×2 + 0,2×3 + 0,2 = 1,4.
⇒ nBr2 phản ứng = 1,4 – nH2 = 1,4 – 0,5 = 0,9 mol.
⇒ mBr2 đã pứ = 0,9 × 160 = 144 gam

Đáp án A
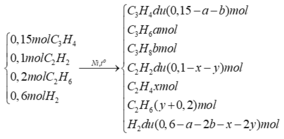
hhY + AgNO3/NH3 → ↓ + 0,7 mol hhZ.
hhY + 0,05 mol Br2
• nBr2 = nC2H4 + nC3H6 = a + x = 0,05.
nankan + nH2du = (b + y + 0,2) + (0,6 - a - 2b - x - 2y) = 0,7 - 0,05
→ b + y = 0,1 mol.
Ta có
∑nY = (0,15 - a - b) + a + b + (0,1 - x - y) + x + (y + 0,2) + (0,6 - a - 2b - x - 2y) = 0,8 mol.
Theo bảo toàn khối lượng:
mY = mX = 0,15 x 40 + 0,1 x 26 + 0,2 x 30 + 0,6 x 2 = 15,8 gam.
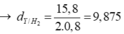
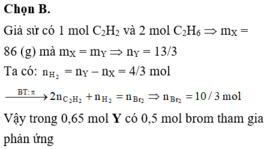
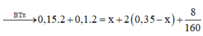
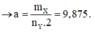

Đáp án A
C2H6 → C2H4 + H2 ;
C2H6 → C2H4 + 2H2
Gọi số mol của etan là : x ;
Bảo toàn khối lượng : mtrước = msau
→ Metan × netan = MX × nX
→ netan = MX × nX : Metan
→ netan = 0,4 × 0,4 = 0,16 (mol)
→ số mol H2 = 0,4 - 0,16 = 0,24 (mol)
Ta thấy H2 được tách ra thì lại được thay bằng Br2 do đó :
nH2 = nBr2 → nBr2 = 0,24 mol