Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Hướng dẫn
Với H = 64,8 % thì số mol của C2H5OH thu được là :

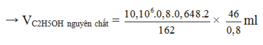
Vậy thể tích dung dịch cồn thực phẩm 40 0 thu được
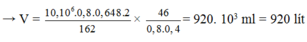

Đáp án: C
Với H = 64,8 % thì số mol của C2H5OH thu được là :


Đáp án : C
n -(-CH2-CH(Cl)-)- =80000 mol
C2H4→CH2Cl−CH2Cl→C2H3Cl→ -(-CH2-CH(Cl)-)-
80000 mol
80%= (80000/n)*100%
=> n ban đầu=100000 mol m C2H4 = 100000*28 = 2800kg

Chọn đáp án B
Ta có 6,2 kg = 6200 g
+ Ta có 1P → 1H3PO4.
⇒ nH3PO4 = nP × 0,8
= 6200 × 0,8 ÷ 31
= 160 mol.
⇒ VH3PO4 = 160 ÷ 2 = 80 lít

Đáp án A
Hướng dẫn C6H5CH3 + 3HONO2 → H 2 SO 4 , t o C6H5(NO2)3CH3 + 3H2O
m = 23 92 .227. 80 100 = 45,4 (kg)

Đáp án C
Hướng dẫn
nPVC = 5000/62,5 = 80 kmol => mC2H4 = 80.100.28/80 = 2800kg

nC2H4 → (-CH2 – CHCl -)n
Theo pt: 28n → 62,5n (kg)
Đề bài: x ← 5000 (kg)
x= 5000.28n/62,5n= 2240 (kg)
H = 80% ⇒ mC2H4 = 2240 : 80% = 2800(kg)
Đáp án C.

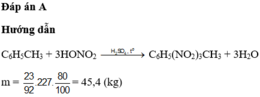
a, nC2H2=10(MOL)
CaC2 + 2H2O → Ca(OH)2 + C2H2
10...............................................10
mCaC2=10.64=640(g)
\(\%m_{CaC_2}=\frac{640}{800}.100\%=80\%\)
b, \(C_2H_2+HCl\xrightarrow[xt]{t^o}CH_2CHCl\)
10.....................................10
\(m_{CH_2CHCl}=10.62,5.\frac{80}{100}=500\left(g\right)\)
CaC2 + 2H2O -----> Ca(OH)2 + C2H2
Theo PT : \(n_{CaC_2\left(lt\right)}=n_{C_2H_2}=10\left(mol\right)\)
\(\Rightarrow\%m_{CaC_2}=\frac{10.64}{800}.100=80\%\)
C2H2 + HCl ----to, xt----> CH2=CH-Cl
Theo PT: \(n_{CH_2=CH-Cl}=n_{C_2H_2}=10\left(mol\right)\)
Vì hiệu suất đạt 80%
\(\Rightarrow m_{CH_2=CH-Cl\left(tt\right)}=10.62,5.80\%=500\left(g\right)=0,5\left(kg\right)\)