Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

C đúng
nH2 = 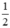 = 0,5 mol.
= 0,5 mol.
Mg + 2HCl → MgCl2 + H2
Fe + 2HCl → FeCl2 + H2
nMg = x; nFe = y.
nH2 = x + y = 0,5 mol.
mhh = 24x + 56y = 20g.
Giải hệ phương trình ta có x = y =0,25 mol.
mMgCl2 = 0, 25 × 95 = 23,75g.
mFeCl2 = 0,25 × 127 = 31,75g
Khối lượng muối clorua = 23,75 + 31,75= 55,5

nH2 = 17.92/22.4 = 0.8 (mol)
nHCl = 2nH2 = 1.6 (mol)
BTKL :
mhh + mHCl = mM + mH2
=> 44.5 + 1.6*36.5 = mM + 0.8*2
=> mM = 101.3 (g)
2 Al + 6 HCl -> 2 AlCl3 + 3 H2
x_____3x______x_____1,5x(mol)
Mg + 2 HCl -> MgCl2 + H2
y__2y________y___y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}27x+24y=44,5\\22,4.1,5x+22,4y=17,92\end{matrix}\right.\)
Anh nhìn đề sai chắc luôn

áp dụng ĐLBT nguyên tố ta có:nH(HCl)=2nH2(bay ra)=1(mol) và nCl(HCl)=nH(HCl)=1(mol).ta có khối lượng muối clorua tạo thành mmuối=mhhKL+mCl(HCl)=20+35.5=55.5(gam)..Chúc bạn học giỏi.

\(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\\n_{Fe}=c\left(mol\right)\end{matrix}\right.\)⇒ 24a + 27b + 56c = 26,05(1)
\(Mg + 2HCl \to MgCl_2 + H_2\\ 2Al +6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = a + 1,5b + c = \dfrac{13,44}{22,4} = 0,6(2)\)
\(Mg + Cl_2 \xrightarrow{t^o} MgCl_2\\ 2Al + 3Cl_2 \xrightarrow{t^o} 2AlCl_3\\ 2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ n_{Cl_2} = a + 1,5b + 1,5c = \dfrac{17,36}{22,4} = 0,775(3)\)
Từ (1)(2)(3) suy ra: a = 0,325 ; b = -0,05 ; c = 0,35
→ Sai đề.

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
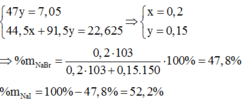


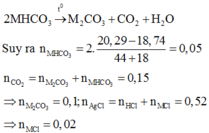



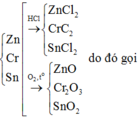
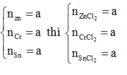

Câu 1:
\(n_{H2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(\Rightarrow n_{HCl}=2n_{H2}=0,5\left(mol\right)=n_{Cl^-}\)
\(\Rightarrow m_{Cl^-}=0,5.35,5=17,75\left(g\right)\)
\(\Rightarrow m_{muoi}=8+17,75=25,75\left(g\right)\)
Câu 2:
\(AgNO_3+NaBr\rightarrow AgBr+NaNO_3\)
\(n_{NaBr}=0,5.0,1=0,05\left(mol\right)\)
\(\Rightarrow n_{AgBr}=n_{NaBr}=0,05\left(mol\right)\)
\(\Rightarrow m_{kt}=0,05.188=9,4\left(g\right)\)
Câu 3:
\(Cl_2+2NaI\rightarrow2NaCl+I_2\)
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(n_{I2}=\frac{12,7}{254}=0,05\left(mol\right)\)
\(\Rightarrow n_{Cl2}=n_{I2}=0,05\left(mol\right)\)
\(\Rightarrow n_{HCl}=4n_{Cl2}=0,2\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,2.36,5=7,3\left(g\right)\)
Bài 1
\(n_{H2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(Mg+2HCl-->MgCl2+H2\)
x------------------------------x-----x(mol)
\(Fe+2HCl-->FeCl2+H2\)
y-----------------------------x--------y(mol)
Theo bài ta có hpt
\(\left\{{}\begin{matrix}24x+56y=8\\x+y=0,25\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1875\\y=0,0625\end{matrix}\right.\)
\(m_{MgCl2}=0,1875.95=17,8125\left(g\right)\)
\(m_{FeCl2}=0,0625.127=7,9375\left(g\right)\)
\(m_{muối}=7,9375+17,8125=25,75\left(g\right)\)
Bài 2
Bài 3
\(4HCl+MnO2-->MnCl2+2H2O+Cl2\)
\(Cl2+2NaI-->2NaCl+I2\)
\(n_{I2}=\frac{12,7}{127}=0,1\left(mol\right)\)
\(n_{Cl2}=n_{I2}=0,1\left(mol\right)\)
\(n_{HCl}=4n_{Cl2}=0,4\left(mol\right)\)
\(m=m_{HCl}=0,4.36,5=14,6\left(g\right)\)