Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{NaCl}=0.5\cdot2=1\left(mol\right)\)
\(n_{AgNO_3}=0.6\cdot2=1.2\left(mol\right)\)
\(AgNO_3+NaCl\rightarrow AgCl+NaNO_3\)
Lập tỉ lệ :
\(\dfrac{1.2}{1}>\dfrac{1}{1}\) \(\Rightarrow AgNO_3dư\)
\(m_{AgCl}=1\cdot143.5=143.5\left(g\right)\)

a)
Xuất hiện kết tủa màu trắng
b)
$AgNO_3 + NaCl \to AgCl + NaNO_3$
$n_{NaCl} = 0,5.2 = 1 < n_{AgNO_3} = 0,6.2 = 1,2$ nên $AgNO_3$ dư
$n_{AgCl} = n_{NaCl} = 1(mol)$
$m_{AgCl} = 1.143,5 = 143,5(gam)$
c)
$n_{NaNO_3} = n_{NaCl} = 1(mol)$
$n_{AgNO_3\ dư} = 1,2 - 1 = 0,2(mol)$
$V_{dd} = 0,5 + 0,6 = 1,1(lít)$
$C_{M_{NaNO_3}} = \dfrac{1}{1,1} = 0,91M$
$C_{M_{AgNO_3}} = \dfrac{0,2}{1,1} = 0,18M$

a) nNaCl=0,4.2=0,8(mol)
nAgNO3= 2.0,6=1,2(mol)
PTHH: NaCl + AgNO3 -> NaNO3 + AgCl (kết tủa)
Ta có: nNaCl(p.ứ)/nNaCl(PT) = 0,8/1 < nAgNO3(p.ứ)/nAgNO3(pt)= 1,2/1
=> P.ứ dư AgNO3, có tạo kt AgCl.
nAgCl= nNaNO3=nAgNO3(P.ứ)=nNaCl= 0,8(mol)
=> m(kết tủa)= mAgCl=0,8. 143,5= 114,8(g)
b) Vddsau= 400+600=1000(ml)=1(l)
CMddNaNO3=0,8/1=0,8(M)
CMddAgNO3(dư)= (1,2-0,8.1)/1= 0,4(M)

\(n_{CuSO_4}=2.0,34=0,68(mol)\\ a,CuSO_4+2NaOH\to Na_2SO_4+Cu(OH)_2\downarrow\\ Cu(OH)_2\xrightarrow{t^o}CuO+H_2O\\ \Rightarrow n_{Cu(OH)_2}=0,68(mol)\\ \Rightarrow m_{Cu(OH)_2}=0,68.98=66,64(g)\\ b,n_{CuO}=0,68(mol)\\ \Rightarrow m_{CuO}=0,68.80=54,4(g)\\ c,V_{dd_{NaOH}}=\dfrac{200}{1,25}=160(ml)\\ n_{NaOH}=\dfrac{200.32\%}{100\%.40}=1,6(mol)\)
Vì \(\dfrac{n_{CuSO_4}}{1}<\dfrac{n_{NaOH}}{2}\) nên \(NaOH\) dư
\(\Rightarrow n_{NaOH(dư)}=1,6-0,68.2=0,24(mol); n_{Na_2SO_4}=0,68(mol)\\ \Rightarrow \begin{cases} C_{M_{NaOH(dư)}}=\dfrac{0,24}{0,16}=1,5M\\ C_{M_{Na_2SO_4}}=\dfrac{0,68}{0,16}=4,25M \end{cases}\)

\(n_{KOH}=0,1.2=0,2mol\\ n_{MgSO_4}=0,1.0,8=0,08mol\\ n_{H_2SO_4}=0,1.0,4=0,04mol\)
Vì bazo và axit luôn pư trc nên H2SO4 hết MgSO4 dư.
\(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
0,08 0,04 0,04 0,08
\(2KOH+MgSO_4\rightarrow Mg\left(OH\right)_2+K_2SO_4\)
0,12 0,06 0,06 0,06
\(Mg\left(OH\right)_2\underrightarrow{t^0}MgO+H_2O\)
0,06 0,06 0,06
\(m_1=m_{Mg\left(OH\right)_2}=0,06.58=3,48g\\ m_2=m_{MgO}=0,06.40=2,4g\\ C_{M\left(K_2SO_4\right)}=\dfrac{0,04+0,06}{0,1+0,1}=0,5M\\ C_{M\left(MgSO_4\right)}=\dfrac{0,08-0,06}{0,1+0,1}=0,1M\)

a)
$FeCl_3 + 3NaOH \to Fe(OH)_3 + 3NaCl$
$2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
$n_{FeCl_3} = 0,3.2 = 0,6(mol)$
Theo PTHH : $n_{Fe_2O_3} = \dfrac{1}{2}n_{FeCl_3} = 0,3(mol)$
$\Rightarrow m_{Fe_2O_3} = 0,3.160 = 48(gam)$
b) Sau phản ứng, $V_{dd} = 0,3 + 0,3 = 0,6(lít)$
$n_{NaCl} = 3n_{FeCl_3} = 1,8(mol) \Rightarrow C_{M_{NaCl}} = \dfrac{1,8}{0,6} = 3M$
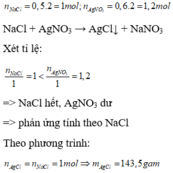

PTHH: \(NaCl+AgNO_3->NaNO_3+AgCl\) Số mol NaCl, \(AgNO_3\) tham gia: \(n_{NaCl}=0,5.2=1\left(mol\right)\) \(n_{AgNO_3}=0,6.2=1,2\left(mol\right)\) Lập tỉ lệ: \(\dfrac{1}{1}< \dfrac{1,2}{1}\) => \(AgNO_3\) dư, tính toán theo NaCl. Theo PTHH: \(n_{AgCl}=n_{NaCl}=1\left(mol\right)\) Khối lượng kết tủa AgCl thu được: \(m_{AgCl}=1.143,5=143,5\left(g\right)\)