Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phân tử lượng B = 2*11,5 = 23
=> B có H2 => KNO3 hếtMg dư
=> H2SO4 hết
số mol Mg phản ứng = mol Mg2+ = (5-0,44)/24 = 0,19
B gồm a mol NO và b mol H2
=> mol B = a + b = 0,08 (1)
khối lượng B = 30a + 2b = 0,08*23 (2) (1) , (2) ==> a = 0,06 và b = 0,02
Mg - 2e ---> Mg2+
0,19--0,38
NO3- + 3e+ 4H+ → NO + 2H2O
0,06-------0,18---0,24-------0,06
2H+ + 2e → H2
0,04------0,04-----0,02
=> mol e nhận = 0,22 < 0,38
=> có muối NH+4 x mol
NO3- + 8e + 10H + → NH4+ + 3H2O
x-------------8x-----10x------------x
Bảo toàn mol e => 0,38 = 0,18 + 0,04 + 8x => x = 0,02 số mol K+ = mol NO−3 = 0,06 + x = 0,08
số mol SO4(2-) = 0,5; mol H+ = 0,5*(0,24 + 0,04 + 10x ) = 0,24
=> Trong dd A có các ion : 0,08 mol K+ , 0,19 mol Mg2+ , 0,02 mol NH4+ và 0,24 mol SO4(2-)
Khối lượng muối = 39*0,08 + 24*0,19 + 18*0,02 + 96*0,24 = 31,08
=> Đáp án C

Đáp án A
Khí B gồm NO ( 0,06 mol ) và H2 ( 0,02 mol ) ; nMg pư = 0,19 mol
Theo định luật bảo toàn electron : nNH4+ = (0,19.2 – 0,06.3 - 0,02.2)/8 = 0,02 mol
Do tạo H2 nên NO3- hết nên : nKNO3 = 0,06 + 0,02 = 0,08 mol
Dung dịch A chứa : Mg2+( 0,19 mol) ; K+ (0,08 mol); NH4+ ( 0,02 mol ) và SO42- ( 0,24 mol )
=> m = 31,08 gam

Đáp án A
Bảo toàn e, bảo toàn điện tích, bảo toàn nguyên tố
Khí B gồm NO (0,06 mol) và H2 (0,02 mol); nMg pư = 0,19 mol
Theo định luật bảo toàn electron: nNH4+ = (0,19.2 – 0,06.3 - 0,02.2)/8 = 0,02 mol
Do tạo H2 nên NO3- hết nên: nKNO3 = 0,06 + 0,02 = 0,08 mol
Dung dịch A chứa: Mg2+(0,19 mol); K+ (0,08 mol); NH4+ (0,02 mol) và SO42- (0,24 mol)
=> m = 31,08 gam

Chọn đáp án D
Ta có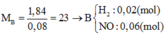
Vì khí B có H2 nên trog dung dịch muối sẽ không có ion NO3-
Ta có
![]()
![]()
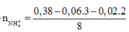
=0,02
![]()
Vậy trong muối có

=>m=29(g)

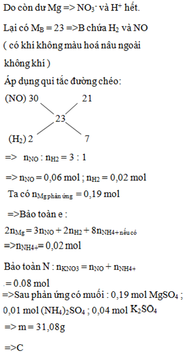
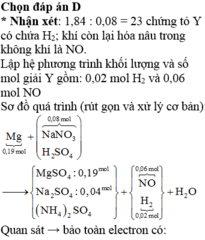

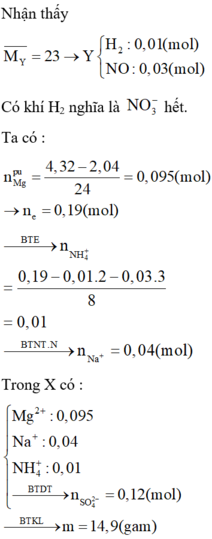
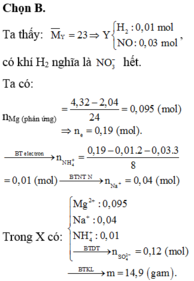
Chọn đáp án C
Ta có:
vì
Chú ý: Có khí H2 bay ra chứng tỏ
trong dung dịch không còn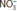
Vậy dung dịch A có: