Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
TH 1: Cả hai muối NaX và NaY đều cho kết tủa khi pư với AgNO3
NaZ + AgNO3 → NaNO3 + AgZ↓
a a
Áp dụng pp tăng giảm khối lượng ![]()
→ a = 0,03 (mol) → MNaZ= 201→ Z = 178
X và Y là I (127) và At (210), nhưng At không có tự nhiên nên TH này loại
TH 2: Chỉ có 1 muối tạo kết tủa nghĩa là hai muối này là NaF và NaCl
nAgCl = 8,61/143,5 = 0,06 mol
NaCl + AgNO3 → NaNO3 + AgCl↓
0,06 0,06
mY = mNaCl = 0,06.58,5 = 3,51g
mX = mNaF = 6,03 - 3,51 = 2,52g
%NaF = ![]() .100% = 41,8%
.100% = 41,8%

Chọn đáp án D
Gỉa sử X không phải Flo
Gọi CTTB của X và Y là X ¯
N a X - + A g N O 3 → A g X - + N a N O 3
23 + X ¯ → 108 + X ¯ (g)
6,03 → 8,61 (g)
8,61.(23 + X ¯ ) = 6,03. (108 + X ¯ )
X ¯ = 175,3 (loại)
X là Flo, Y là Clo
Kết tủa chỉ gồm AgCl; n A g C l = n N a C l = 8,61 : 143,5 = 0,06 mol
% m N a C l = 0 , 06 . 58 , 5 6 , 03 . 100 = 58,2 (%) → % m N a F = 41,8 (%).

TH1: NaF và NaCl
Kết tủa chỉ có AgCl
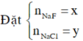
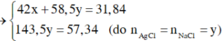
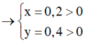
Vậy CT 2 muối có thể là NaF và NaCl
TH2: Hỗn hợp muối không chứa NaF
Đặt CT chung của 2 muối ban đầu là NaX
![]()
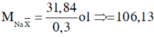
=> 2 muối là NaBr và NaI
Đáp án A

Chọn A
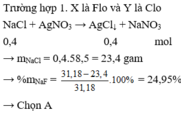
Chú ý: Với đề trắc nghiệm chọn được đáp án A có thể không cần xét thêm trường hợp 2.
Trường hợp 2. X khác Flo. Gọi hỗn hợp (NaX, NaY) tương đương với NaM


Đáp án A.
Hỗn hợp (NaX, NaY) = NaM
NaM + AgNO3 → AgM↓+NaNO3
Ta có
![]() => M = 81,6 => X,Y lần lượt là Br (80) và I (127)
=> M = 81,6 => X,Y lần lượt là Br (80) và I (127)

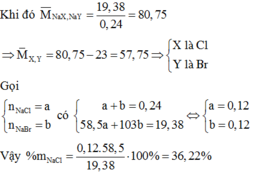


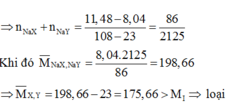
a) Giả sử MX < MY
TH1: Nếu trong hỗn hợp có NaF
=> muối còn lại là NaCl
\(n_{AgCl}=\dfrac{57,4}{143,5}=0,4\left(mol\right)\)
=> nNaCl = 0,4 (mol)
=> mNaCl = 0,4.58,5 = 23,4 (g)
\(\%m_{NaCl}=\dfrac{23,4}{31,9}.100\%=73,35\%\)
\(\%m_{NaF}=\dfrac{31,9-23,4}{31,9}.100\%=26,65\%\)
TH2: Nễu trong hh không có NaF
Gọi công thức chung của 2 muối là NaZ
\(n_{AgZ}=\dfrac{57,4}{108+M_Z}\left(mol\right)\)
=> \(n_{NaZ}=\dfrac{31,9}{23+M_Z}=\dfrac{57,4}{108+M_Z}\)
=> MZ = 83,333 (g/mol)
=> NaX, NaY lần lượt là NaBr, NaI
Gọi \(\left\{{}\begin{matrix}n_{NaBr}=a\left(mol\right)\\n_{NaI}=b\left(mol\right)\end{matrix}\right.\)
=> 103a + 150b = 31,9 (1)
\(\left\{{}\begin{matrix}n_{AgBr}=a\left(mol\right)\\n_{AgI}=b\left(mol\right)\end{matrix}\right.\)
=> 188a + 235b = 57,4 (2)
(1)(2) => \(\left\{{}\begin{matrix}a=\dfrac{131}{470}\left(mol\right)\\b=\dfrac{1}{47}\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{NaBr}=\dfrac{\dfrac{131}{470}.103}{31,9}.100\%=90\%\\\%m_{NaI}=\dfrac{\dfrac{1}{47}.150}{31,9}.100\%=10\%\end{matrix}\right.\)
b)
TH1: Nếu là NaF và NaCl
- Cho các dd tác dụng với dd AgNO3:
+ Không hiện tượng: NaF
+ Kết tủa trắng: NaCl
NaCl + AgNO3 --> NaNO3 + AgCl
TH2: Nếu là NaBr và NaI
- Cho các dd tác dụng với dd AgNO3:
+ Kết tủa vàng nhạt: NaBr
NaBr + AgNO3 --> AgBr + NaNO3
+ Kết tủa vàng: NaI
NaI + AgNO3 --> AgI + NaNO3