Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
a 0,4 0,2 1a
\(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
b 0,3 0,15 1b
a) Gọi a là số mol của Mg
b là số mol của Fe
\(m_{Mg}+m_{Fe}=13,2\left(g\right)\)
⇒ \(n_{Mg}.M_{Mg}+n_{Fe}.M_{Fe}=13,2g\)
⇒ 24a + 56b = 13,2g (1)
Theo phương trình : 1a + 1b = 0,35(2)
Từ(1),(2), ta có hệ phương trình :
24a + 56b = 13,2g
1a + 1b = 0,35
⇒ \(\left\{{}\begin{matrix}a=0,2\\b=0,15\end{matrix}\right.\)
\(m_{Mg}=0,2.24=4,8\left(g\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
0/0Mg = \(\dfrac{4,8.100}{13,2}=36,36\)0/0
0/0Fe = \(\dfrac{8,4.100}{13,2}=63,64\)0/0
b) \(n_{HCl\left(tổng\right)}=0,4+0,3=0,7\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddHCl}}=\dfrac{0,7}{0,2}=3,5\left(M\right)\)
c) \(m_{muối.clorua}=\left(0,2.95\right)+\left(0,15.127\right)=38,05\left(g\right)\)
Chúc bạn học tốt

\(n_{Cu_2S}=n_{FeS}=a\left(mol\right)\\ 160a+88a=24,8\left(g\right)\\ \rightarrow n_{Cu_2S}=n_{FeS}=0,1\left(mol\right)\)
PTHH:
Cu2S + 6H2SO4 ---> 2CuSO4 + 5SO2 + 6H2O
0,1 ------> 0,6 ----------> 0,2 ------> 0,5 ------> 0,6
2FeS + 10H2SO4 ---> Fe2(SO4)3 + 9SO2 + 10H2O
0,1 ------> 0,5 -----------> 0,05 --------> 0,45 ---> 0,5
\(\rightarrow\left\{{}\begin{matrix}V_{SO_2}=\left(0,5+0,45\right).22,4=21,28\left(l\right)\\n_{H_2SO_4}=0,5+0,6=1,1\left(mol\right)\end{matrix}\right.\)
PTHH:
Fe2(SO4)3 + 6KOH ---> 2Fe(OH)3 + 3K2SO4
0,05 ------------------------> 0,1
CuSO4 + 2KOH ---> Cu(OH)2 + K2SO4
0,2 -----------------------> 0,2
2Fe(OH)3 --to--> Fe2O3 + 3H2O
0,1 ------------------> 0,05
Cu(OH)2 --to--> CuO + H2O
0,2 ----------------> 0,2
\(\rightarrow\left\{{}\begin{matrix}m=107.0,1+98.0,2=20,5\left(g\right)\\a=0,05.160+0,2.80=24\left(g\right)\end{matrix}\right.\)

a)\(\left\{{}\begin{matrix}Fe:a\left(mol\right)\\Al:b\left(mol\right)\end{matrix}\right.\)⇒ 56a + 27b = 1,93(1)
\(Fe + 2HCl \to FeCl_2 + H_2\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\)
Theo PTHH : a + 1,5b = \(\dfrac{1,456}{22,4} = 0,065\)(2)
Từ (1)(2) suy ra : a = 0,02 ; b = 0,03
Vậy :
\(\%m_{Fe} = \dfrac{0,02.56}{1,93}.100\% = 58,03\%\\ \%m_{Al} = 100\% - 58,03\% = 41,97\%\)
b)
\(C_{M_{FeCl_2}} = \dfrac{0,02}{0,2} = 0,1M\\ C_{M_{AlCl_3}} = \dfrac{0,03}{0,2} = 0,15M\)
c)
\(n_{HCl} = 2n_{H_2} = 0,065.2 = 0,13(mol)\\ a = \dfrac{0,13}{0,2} = 0,65(M)\)

Phần 1:
Fe + 2HCl → FeCl2 + H2
nH2 = 4,48:22,4 = 0,2 mol = nFe
<=> mFe = 0,2.56 = 11,2 gam
=> mCu = 35,2:2 - 11,2 = 0,1 mol
Phần 2:
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
=> nSO2 = 0,3 + 0,1 = 0,4 mol <=> V = 0,4.22,4 = 8,96 lít
=>nH2SO4 phản ứng = 3.0,2 + 2.0,1 = 0,8 mol
=> nH2SO4 ban đầu = 0,8 + 0,8.15% = 0,92 mol
<=>m dung dịch = m(Fe + Cu) + mH2SO4 - mSO2 = 35,2:2 + 0,92.98 - 0,4.64 = 82,16 gam
C%Fe2(SO4)3 = \(\dfrac{0,1.400}{82,16}.100\%\)= 48,7%
C%CuSO4 = \(\dfrac{0,1.160}{82,16}.100\%\) = 19,5%
C%H2SO4 dư = \(\dfrac{0,8.15\%.98}{82,16}\).100% = 14,7%

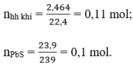
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) Theo PT (2) ⇒ nFeS = nH2S = 0,1 mol
⇒ mFeS = 0,1 × 88 = 8,8g.
Theo PT (1) nFe = nH2 = 0,01 mol ⇒ mFe = 56 × 0,01 = 0,56g.
Gọi số mol HCl và H2So4 lần lượt là x, y
Cho hỗn hợp axit tác dụng với Fe dư thu được 0,2 mol khí H2
\(\Rightarrow x+2y=n_{H2}.2=0,4\)
Lấy 1/10 dung dịch A chứa 0,1y mol SO42-.
Cho dung dịch này tác dụng với BaCl2 thu được kết tủa là BaSO4
\(n_{BaSO4}=0,1y=\frac{2,33}{233}=0,01\left(mol\right)\Rightarrow y=0,1\left(mol\right)\)
\(\Rightarrow x=0,2\)
\(\Rightarrow CM_{HCl}=\frac{0,2}{0,2}=1M\)
\(\Rightarrow CM_{H2SO4}=\frac{0,1}{0,2}=0,5M\)
Ta có:
\(n_{Fe}=n_{H2}=0,2\left(mol\right)\Rightarrow m_{Fe}=11,2\left(g\right)\)