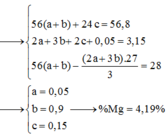Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
2Al + 6H+ → 2Al3+ + 3H2
0,1 ←0,3 ← 0,15
[Al(OH)4]- + 4H+→ Al3+ + 4H2O
0,125 ← (0,8 – 0,3)
Al + OH- + 3H2O →[Al(OH)4]- + 3/2 H2
0,125 ← 0,125 ← 0,125
⇒ m = (0,125 + 0,1).27 = 6,075 g
⇒V dd NaOH = 0,125/ 2 = 0,0625 lít

Đáp án D
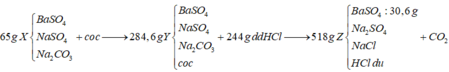
Bảo toàn khối lượng => mCO2 = mY + mddHCl - mZ
=> mCO2 = 284,6 + 244 – 518 = 10,6 (g)
=> nCO2 = 0,241
Tại 200 g ddHCl thì không có khí thoát ra nữa => HCl dư, Na2CO3 phản ứng hết
BTNT C=> nNa2CO3 = nCO2 = 0,241 (mol)
BTKL => mNa2SO4 = mX – mBaSO4 – mNa2CO3 = 65 – 30,6 – 0,241.106 = 8,854 (g)
% Na2CO3 = (8,854/ 65).100% = 13,62%
Gần nhất với giá trị 13,5%

Chọn C.
Cốc 3, 4 đều xảy ra ăn mòn điện hóa nhưng cốc 4 bị ăn mòn nhanh hơn vì Zn có tính khử mạnh hơn Fe.
Cốc 1, 2 đều xảy ra ăn mòn hóa học nhưng do Zn có tính khử mạnh hơn Fe nên cốc 1 bị ăn mòn nhanh hơn cốc 2.
Vì ăn mòn điện hóa thì kim loại bị ăn mòn nhanh hơn so với lại ăn mòn hóa học nên tốc độ giải phóng khí giảm dần theo thứ tự (4) > (3) > (1) > (2).

Đáp án A
• (1)0,3 mol NaOH + 0,1x mol AlCl3 → 0,1 mol Al(OH)3↓
(2)Thêm tiếp 0,2 mol NaOH → 0,14 mol Al(OH)3↓
→ Giai đoạn (1) kết tủa chưa tan; (2) kết tủa tan một phần
• 3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl (*)
Al(OH)3 + NaOHdư → NaAlO2 + 2H2O
Theo (*) nNaOH = 3 × nAlCl3 = 3 × 0,1x = 0,3x mol; nAl(OH)3 = 0,1x mol.
Theo (**) nAl(OH)3 phản ứng = 0,1x - 0,14 mol → nNaOH = 0,1x - 0,14 mol
→ ∑nNaOH = 0,3x + 0,1x - 0,14 = 0,3 + 0,2 → x = 1,6

Đáp án C.
TN1: 150 ml dd Y (NaOH 2M) vào 100 ml dd X (AlCl3) à 7,8 gam kết tủa Al(OH)3
TN2: Thêm tiếp vào cốc trên 100 ml dd Y à 10,92 gam kết tủa Al(OH)3
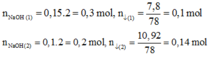



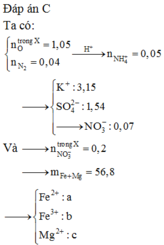
Đáp án C
nHNO3 = 0,68; nNO = 0,12
nHNO3 = 4nNO+ 10nNH4NO3=> nNH4NO3 = 0,02 => ne = 3nNO + 8nNH4NO3 = 0,52
mmuối = mkim loại + 62ne + mNH4NO3=> 2,5m + 8,49 = m + 62.0,52 + 80.0,02 => m = 16,9
Bảo toàn ne=>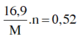 =>
=>