Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) PTPỨ: \(SO_2+NaOH\rightarrow NaHSO_3\)
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
b) \(n_{SO_2}=0,2\left(mol\right);n_{NaOH}=1.0,25=0,25\left(mol\right)\)
\(\Rightarrow\frac{n_{NaOH}}{n_{SO_2}}=\frac{0,25}{0,2}=1,25\)
\(SO_2+NaOH\rightarrow NaHSO_3\)
a a a
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
b 2b b
\(\Rightarrow\left\{{}\begin{matrix}a+b=0,2\\a+2b=0,25\end{matrix}\right.\)
Giải ra ta được: \(a=0,15mol;b=0,05mol\)
\(\rightarrow m_{Na_2SO_3}=0,05\left(23,2+32+48\right)=6,3\left(g\right)\)
\(\rightarrow m_{NaHSO_3}=0,15\left(23+1+32+48\right)=15,6\left(g\right)\)

a)NaOH+SO2 \(\rightarrow\) NaHSO3 (1)
NaOH+SO2 \(\rightarrow\) Na2SO3+H2O (2)
b)Ta có co số mol SO2 là : n = 12,8 / 64 = 0,2
số mol NAOH là : n =0,25 x 1 = 0,25
Ta có tỷ lệ :
n [NaOH]/ n [SO2] = 0,25/0,2 = 1,25
Nên sẽ xảy ra đồng thời 2 phản ứng 1 và 2
NaOH + SO2 = NaHSO3 (1)
x mol x mol x mol
2NaOH + SO2 = Na2So3 + H2O (2)
y mol y/2 mol y/2 mol
Từ (1)(2): Ta có hệ phương trình :
x+y = 0,25
x+y/2 = 0,2
Giải hệ trên ta có x = 0,15 mol
y= 0,1 mol
Khối lượng muối sau phản ứng sẽ bao gồm 2 muối là NaHSO3 và NA2SO3
Số mol Nahso3 = x = 0,15 mol
==> Khối lương NAHSO3 = 0,15 x 104 = 15,6 g
Số mol NA2SO3 = y/2 = 0,1 /2 = 0,05 mol
==> Khối lượng NA2SO3 = 0,05 x 126 = 6,3 g
Vậy khối lượng muối thu dc sau phản ứng là : 15,6 + 6,3 = 21,9 g

Cu +2H2SO4----> CuSO4+SO2+2H2O
nSO2=nCu=12,8/64=0,2 mol.
nNaOH=(125.1,28.25)/100=40 gam =>nNaOH=1 mol
nNaOH/nSO2=1/0,2=5 tạo ra muối Natrisunfit Na2SO3
nNa2SO3=nSO2=0,2=> CMNa2SO3=0,2/0,125=1,6 M.

1. Số mol SO2 và NaOH lần lượt là 150.3,4%:64=51/640 (mol) và 0,25.1=0,25 (mol).
\(\dfrac{n_{OH^-}}{n_{SO_2}}\approx3,127>2\) \(\Rightarrow\) Muối thu được chỉ có Na2SO3 (51/640 mol) có khối lượng là 51/640.126=3213/320 (g).
2. FeS + 2HCl (913/9125 mol) \(\rightarrow\) FeCl2 + H2S\(\uparrow\) (913/18250 mol).
2H2S (913/18250 mol) + 3O2 \(\underrightarrow{t^o}\) 2SO2\(\uparrow\) (913/18250 mol) + 2H2O.
Số mol FeS, HCl và NaOH lần lượt là 10:88=5/44 (mol), (20%.1,1.16,6:100%):36,5=913/9125 (mol) và 0,5.0,1=0,05 (mol).
\(\dfrac{n_{OH^-}}{n_{SO_2}}\approx0,9995< 1\) \(\Rightarrow\) Muối thu được chỉ là natri hiđrosunfit hay natri bisunfit (NaHSO3 0,05 mol) có nồng độ mol là 0,05/0,5=0,1 (mol/l).

SO2+NaOH->NaHSO3
n So2=0,05 mol
Giả sử phản ứng tạo 1 muối NaHSO3
BTNT S: nNaHSO3 = nSO2 = 0,05 => m muối = 5,2 gam < 5,75 gam
Giả sử phản ứng tạo 1 muối Na2SO3
BTNT S: nNa2SO3 = nSO2 = 0,05 => m muối = 6,3 gam > 5,75 gam
Chứng tỏ phản ứng tạo hỗn hợp 2 muối NaHSO3 (a mol) và Na2SO3 (b mol)
\(\left\{{}\begin{matrix}a+b=0,05\\\text{104 a + 126 b = 5,75 }\end{matrix}\right.\)
a=0,025, b=0,025 mol
BTNT Na => n NaOH = 2n Na2SO3 + n NaHSO3 = 0,075 mol
VNaOH = 0,075 :1 = 0,075 lít = 75ml
SO2 + NaOH ---> \(\left[{}\begin{matrix}Na2SO3+H2O\\NaHSO3\end{matrix}\right.\)
nSO2 = \(\dfrac{3,2}{64}=0,05\left(mol\right)\)
Bảo toàn nguyên tố : nSO2 = nS (muối) = 0,05 (mol)
M (muối) = \(\dfrac{5,75}{0,05}=115\left(đvC\right)\)
Nhận thấy MNaHSO3 < M(muối) < MNa2SO3
=> Phản ứng tạo 2 muối
Gọi muối NaHSO3 là x , Na2SO3 là y
Ta có : \(\left\{{}\begin{matrix}x+y=0,05\\104x+126y=5,75\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,025\\y=0,025\end{matrix}\right.\)
Bảo toàn Na : 0,025.1 + 0,025.2 = 0,075 ( mol )
=> V NaOH = n/Cm = 75 ( ml )

Câu 2.Hấp thụ hoàn toàn 12,8 gam SO2 vào 250 ml dung dịch NaOH 1M.
a) Viết các phương trình hóa học của phản ứng xảy ra. b) Tính khối lượng muối tạo thành sau phản ứng.
----
a) nSO2= 12,8/64= 0,2(mol)
nNaOH= 0,25.1=0,25(mol)
Ta có tỉ lệ: 1< nNaOH/nSO2= 0,25/0,2=1,25 <2
=> Tạo 2 muối: Na2CO3 và NaHCO3
Gọi x, y lần lượt là số mol NaOH (1) và NaOH (2)
PTHH: 2 NaOH + CO2 -> Na2CO3 + H2O (1)
x______________0,5x___0,5x(mol)
NaOH+CO2 -> NaHCO3 (2)
y______y_____y(mol)
=> \(\left\{{}\begin{matrix}x+y=0,25\\0,5x+y=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\)
b) =>mNa2CO3=0,5.106x=0,5.106.0,1= 5,3(g)
mNaHCO3=0,15.84= 12,3(g)
-> m(muối)= mNa2CO3+ mNaHCO3= 5,3+12,3= 17,6(g)
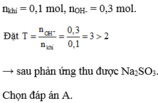


ta có số mol của SO2 bằng\(\dfrac{12,8}{64}\)=0,2
số mol của NaOH bằng\(\dfrac{0,25}{1}\)=0,25
khi đó ta có \(\dfrac{0,25}{0,2}\)=1,25 1<1,25<2 => khi phản ứng tạo ra 2 muối: trung hòa và axit
PTHH SO2 + 2 NaOH -----> Na2SO3 + H2O (1)
SO2 + NaOH ------> NaHSO3 (2)
gọi x là số mol của SO2 ở PTHH (1)
y là số mol của SO2 ở PTHH (2)
khi đó ta có hệ pt
\(\left\{{}\begin{matrix}x+y=0,2\\2x+y=0,25\end{matrix}\right.\)====> \(\left\{{}\begin{matrix}x=0,05\\y=0,15\end{matrix}\right.\)
suy ra khối lượng của NaHSO3 = 0,15*104=15,6(g)
khối lượng của Na2SO3 = 0,05*126=6,3(g)
nSO2=0,2mol, nNaOH=0,25mol
T=\(\dfrac{0,25}{0,2}\) =1,25 tạo hai muối
SO2 + NaOH -------> NaHCO3
x mol xmol
SO2 +2 NaOH-------> Na2CO3 + H2O
y mol 2y mol
\(\left\{{}\begin{matrix}x+y=0,2\\x+2y=0,25\end{matrix}\right.\) \(\left\{{}\begin{matrix}x=0,15\\y=0,05\end{matrix}\right.\)
Khối lượng muối tạo thành
m=mNaHCO3+mNa2Co3=17,9g