Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

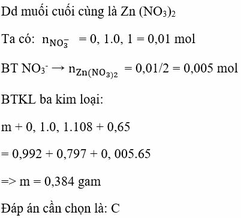
Đáp án C
GIẢ SỬ Ag+ bị “đẩy” ra hết ![]()
=> chất rắn sau phản ứng chứa Fe dư. Đặt n F e phản ứng = x, n A l = y
4Fe dư => X chứa ![]()
![]()
Bảo toàn khối lượng gốc kim loại: 0,42 + 0,03 x 108 = 56x + 27y = 3,333
=> Giải hệ có: x = 0,0015 mol; y = 0,009 mol; ![]()
=> Chọn C

Đáp án C
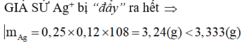
=> chất rắn sau phản ứng chứa Fe dư. Đặt
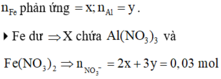
Bảo toàn khối lượng gốc kim loại:
![]()
=> giải hệ có: x = 0,0015 mol; y = 0,009 mol
![]()

Đáp án A
Gọi nZn = a; nFe = b thì nCu = a + b
Vì khối lượng chất rắn trước và sau phản ứng bằng nhau nên mZn + mFe = mCu
Do đó 65a + 56b = 64(a+b) ⇔ a = 8b
Vậy phần trăm khối lượng cúa Zn trong hỗn hợp ban đầu là:
% m Z n = 65 . 8 b 65 . 8 b + 56 b . 100 % = 90 , 27 %

CuSO4 → KL pư hết.
Gọi: \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\) ⇒ m = 65a + 56b (1)
BT e, có: 2a + 2b = 2nCu ⇒ nCu = a + b (mol) ⇒ m = 64(a + b) (2)
Từ (1) và (2) ⇒ 65a + 56b = 64a + 64b
⇒ a = 8b
\(\Rightarrow\%m_{Zn}=\dfrac{65a}{65a+56b}.100\%=\dfrac{65.8b}{65.8b+56b}.100\%\approx90,28\%\)