Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.d_{\dfrac{X_2}{O_2}}=2,218\\ m_{O_2}=32\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_{X_2}=32.2,218=71\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_X=\dfrac{71}{2}=35,5\left(\dfrac{g}{mol}\right)\\ \Rightarrow X.là.Clo\)
\(b.d_{\dfrac{Cl_2}{kk}}=\dfrac{71}{29}\approx2,4>1\\ \Rightarrow thu.bằng.pp.đặt.bình.đứng\)

1
a) Khối lượng mol phân tử của khí Z là :
dZ/H2 = MZ / MH2= 22 ( g )
=> MZ = dZ/H2 x MH2 = 22x2 = 44 g
b) Công thức phân tử của khí Z là : N2O
c) dZ/KK = Mz / MKK = 44/29 = 1,52 ( lần )
2.
dA/B = mA/mB là đúng vì :
Biết V => n => m => M
3.
a ) Kim đồng hồ sẽ ko lệch về bên nào cả, nó đứng ở vị trí chính giữa
b) Nếu không làm thí nghiệm, có thể dự đoán đc kim đồng hồ sẽ lệch về bên nào.
MKK = 0,8 + 0,2 = 1 mol = 29 g

Câu 5:
\(a,m_{CaCl_2}=n_{CaCl_2}.M_{CaCl_2}=0,2.111=22,2\left(g\right)\\ b,n_{CO_2\left(ĐKC\right)}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
Câu 6: Úp đứng bình vì khí O2 nặng hơn không khí. (32>29)

Hidro nhẹ hơn không khí vì (d\(\dfrac{H_2}{kk}\)= \(\dfrac{2}{29}\)<1)
Oxi nặng hơn không khí vì (d\(\dfrac{O_2}{kk}\)=\(\dfrac{32}{29}\)>1)
Để thu được khí hidro khi điều chế cần đặt úp bình vì khí hidro nhẹ hơn không khí ,nếu ngửa bình hidro sẽ bay ra khỏi bình .
Ngược lại để thu được khí oxi khi điều chế cần ngửa bình vì oxi nặng hơn không khí sẽ lắng xuống đáy bình , nếu úp bình oxi sẽ lắng xuống và thoát ra khỏi bình

Xác định X, Y biết rằng:
- Hợp chất X2O có PTK là 62
=> X hóa trị I
- Hợp chất YH2 có PTK là 34.
=> Y hóa trị II
=> Công thức đúng cho hợp chất của X và Y là X2Y

Ta có:
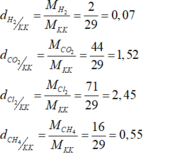
a) Đặt ngửa bình thu được những khí có tỉ khối đối với không khí lớn hơn 1
- Khí clo nặng hơn không khí 2,45 lần
- Khí cacbon đioxit nặng hơn không khí 1,52 lần
b) Đặt úp bình thu được những khí còn lại có tỉ khối đối với không khí nhỏ hơn 1:
- Khí hiđro nhẹ hơn không khí và bằng 0,07 lần không khí
- Khí metan CH4 nhẹ hơn không khí và bằng 0,55 lần không khí.

a/ Khối lượng mol của khí X2O: c/Tỉ khối của khí N2O đối với kk
\(M_{X2O}=d_{x2o}.M_{O2}=1.375\cdot32=44\)(g/mol) dN2O/kk= \(\frac{M_{N2O}}{29}\) =\(\frac{44}{29}\) =1.5
Ta có: MX2O=MX2+MO=44 Vậy khí N2O nặng hơn kk 1.5 lần. Do đó khí N2O phải được đặt đứng bình.
\(\Rightarrow M_{X2}=44-M_O=44-16=28\)
\(\Rightarrow M_X=14\)
\(\Rightarrow X\)là nguyên tố N.
b/Thể tích khí N2O của 0.25 mol ở đktc
VN2O= n*22.4=0.25*22.4=5.6 (lít)
Thể tích khí N2O của 0.25 mol ở đkt
VN2O=n*24=0.25*24=6(l)
câu c cách ra dùm chút nhen. hết chỗ ghi rồi