Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

gọi số prton,electron và notron của X lần lượt là :p,e,n
do p=e=> p+e=2p
theo đề ta có hpt: \(\begin{cases}2p+n=52\\2p=1,889n\end{cases}\)
<=> \(\begin{cases}p=17\\n=18\end{cases}\)
do p=17
=> x là Clo (Cl)
Cl nằm ở ô thứ 17 trong BTH

Đáp án D
Hai nguyên tố thuộc cùng một nhóm A, thuộc hai chu kỳ liên tiếp = Điện tích hạt nhân cách nhau 8, 18 hay 32
Trường hợp 1:
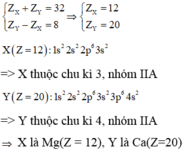
Trường hợp 2:
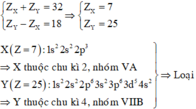
Trường hợp 3:
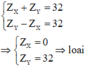

Vì 2 nguyên tố X, Y thuộc 2 nhóm A liên tiếp nên: \(\left\{{}\begin{matrix}Z_X+Z_Y=39\\Z_Y-Z_X=1\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}Z_X=19\\Z_Y=20\end{matrix}\right.\)
ZX=19 => Cấu hình e: \(1s^22s^22p^63s^23p^64s^1\)
=> X thuộc ô 19 là Kali (K), nhóm IA, chu kỳ IV
ZX=20 => Cấu hình e: \(1s^22s^22p^63s^23p^64s^2\)
=> X thuộc ô 20 là Canxi (Ca), nhóm IIA, chu kỳ IV

a) Trong cùng 1 chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử của nguyên tố giảm dần \(\Rightarrow Z_X< X_Y\).
-Vì 2 nguyên tố X,Y đứng kế nhau trong bảng tuần hoàn nên \(Z_X+1=Z_Y\left(1\right)\)
-Vì 2 nguyên tố X,Y có tổng số hạt mang điện là 58 nên \(2\left(Z_X+Z_Y\right)=58\left(2\right)\)
Từ (1), (2) ta có: \(\left\{{}\begin{matrix}Z_X=14\\Z_Y=15\end{matrix}\right.\)
Cấu hình electron của nguyên tử X,Y:
\(X:1s^22s^22p^63s^23p^2\) ; \(Y:1s^22s^22p^63s^23p^3\)
b) Vị trí của X,Y trong bảng tuần hoàn:
X: ô 14, nhóm IVA, chu kì 3. X là Si.
Y: ô 15, nhóm VA, chu kì 3. Y là P.