Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(\dfrac{n_t}{n_s}=\dfrac{M_s}{M_t}\Rightarrow\dfrac{1}{3}=\dfrac{12.2}{M_t}\Rightarrow M_t=72\)
Do đó X là $C_5H_{12}$
Khi mono clo hóa thu được $C_5H_{11}Cl$
$\Rightarrow \%m_{Cl}=33,3\%$
Khi monoclo hoá thu đc C5H11cl là sao vậy ạ ? E chưa rõ lắm đoạn này lắm:((

Chọn đáp án C
Y : C u C u O + → + H N O 3 0,4 mol NO
n C u = 3 2 . n N O = 0,6 mol
C O H 2 + O C u O → C u
n C O + n H 2 = n [ O ] C u O = n C u = 0,6 mol. Gọi n C O = x mol; n H 2 = y mol
x + y = 0,6 (1) => n C O 2 = 0,7 – 0,6 = 0,1 mol
Bảo toàn C và H ta có: n H 2 = n H 2 O = n [ O ] H 2 O = 2 n C O 2 + nCO
y = 2.0,1 + x => y – x = 0,2 mol (2)
Từ (1)(2) => x = 0,2; y = 0,4
% V C O = 0 , 2 0 , 7 .100% = 28,57%

a) Ankan có CTPT dạng (C2H5)n => C2nH5n
Vì là ankan nên: 5n = 2n x 2 + 2 => n = 2
Vậy CTCT của Y là CH3– CH2– CH2– CH3 (butan)
b) CH3– CH2– CH2– CH3 + Cl2
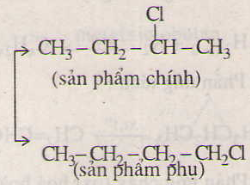
+ HCl

1. Trong 1000 m 3 khí thiên nhiên có 850 m 3 C H 4
2 C H 4 → 1500 ° C C 2 H 2 + 3 H 2
CH ≡ CH + HCl → 150 - 200 ° C , H g C l 2 C H 2 = C H - C l
Khối lượng vinyl clorua thu được (nếu hiệu suất các quá trình là 100%) là:
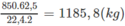
Với hiệu suất cho ở đầu bài, khối lượng vinyl clorua là:
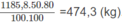
2. Nhiệt lượng cần dùng để làm nóng 100 lít nước từ 20 ° C lên 100 ° C :
100.4,18.(100 - 20) = 33440 (kJ)
Vì 20% nhiệt lượng đã toả ra môi trường nên nhiệt lượng mà khí thiên nhiên cần cung cấp phải là :
Đặt số mol C 2 H 6 tà x thì số mol C H 4 là 85. 10 - 1 x.
Ta có 1560x + 88085. 10 - 1 x = 41800
x = 462. 10 - 2
Thể tích khí thiên nhiên cần dùng:
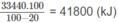

Đáp án D
Đốt cháy hỗn hợp gồm SiH4 và CH4 thu được chất rắn là SiO2 và chất khí là CO2.
Ta có: SiH4+2 O2 → SiO2+ 2H2O
CH4+2 O2 → CO2+ 2H2O
Ta có: nSiH4= nSiO2= 6/60= 0,1 mol
Khi cho khí CO2 qua dung dịch NaOH dư thì:
CO2+ 2NaOH → Na2CO3+ H2O
Theo PTHH: nCH4= nCO2=nNa2CO3= 31,8/106= 0,3 mol
→ nX= nCH4+ nSiH4= 0,3 + 0,1= 0,4 mol
Trong cùng điều kiện, tỉ lệ về số mol chính là tỉ lệ về thể tích
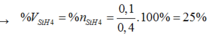
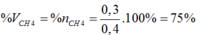

Số mol
O
2
: 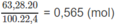
Số mol C O 2 = số mol C a C O 3 = 0,36 (mol).
1. Trong 0,36 mol C O 2 , khối lượng cacbon: 0,36 x 12 = 4,32 (g) và khối lượng oxi: 0,36 x 32 = 11,52 (g).
Khối lượng oxi trong nước là: 0,565 x 32,0 - 11,52 = 6,56 (g).
Khối lương hiđro (trong nước): 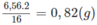
Khối lượng M = khối lượng C + khối lượng H = 4,32 + 0,82 = 5,14 (g)
2. Khi đốt 1 mol ankan, số mol H 2 O tạo ra nhiều hơn số mol C O 2 là 1 mol. Khi đốt hỗn hợp M, số mol H 2 O nhiều hơn số mol C O 2 :
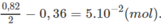
Vậy hỗn hợp M có 5. 10 - 2 mol ankan.
Khối lượng trung bình của 1 mol ankan:
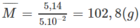
14n + 2 < 102,8 < 14n + 30
⇒ 5,20 < n < 7,20
Đến đây có thể tìm được công thức phân tử và phần trăm khối lượng từng chất như ở cách thứ nhất.

1. Khi đun nóng A có mặt chất xúc tác Ni, chỉ còn lại 1 chất khí duy nhất. Vậy ankan và anken trong A có cùng số nguyên tử cacbon.
Giả sử trong 100 ml A có x mol C n H 2 n + 2 ; y mol C n H 2 n và z mol H 2 .
x + y + z = 100 (1)
Khi đốt cháy hoàn toàn 100 ml A :
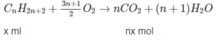
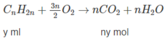
2 H 2 + O 2 → 2 H 2 O
Thể tích C O 2 : n(x + y) = 210 (2)
Khi đun nóng A có mặt chất xúc tác Ni:
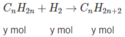
x + y = 70 (3)
y = z (4)
Giải hộ phương trình, tìm được n = 3; x = 40 ; y = z = 30.
Thành phần thể tích của hỗn hợp A là : C 3 H 8 : 40% ; C 3 H 6 : 30%; H 2 : 30%
2. Thể tích O 2 là 350 ml.

- Gọi mol metan và etan là x, y ( mol )
\(x+y=n_{hh}=\dfrac{V}{22,4}=0,25\left(mol\right)\)
Lại có : \(x+2y=n_{CO_2}=\dfrac{V}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\) ( mol )
\(\Rightarrow\left\{{}\begin{matrix}m_{CH_4}=1,6\left(g\right)\\m_{C_2H_6}=4,5\left(g\right)\end{matrix}\right.\)
=> mhh = 6,1 ( g )
=> %mCH4 = ~ 26,22%
=> %mC2H6 = ~73,78%
Ta có : \(\%V_{CH4}=\dfrac{V}{Vhh}=40\%\)
=> %VC2H6 = 100 - %VCH4 = 60% .
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_6+5O_2\underrightarrow{t^o}4CO_2+6H_2O\)
Giả sử: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_6}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{5,6}{22,4}=0,25\left(1\right)\)
Ta có: \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(\Sigma n_{CO_2}=n_{CH_4}+2n_{C_2H_6}\)
\(\Rightarrow x+2y=0,4\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,25}.100\%=40\%\\\%V_{C_2H_6}=60\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,1.16}{0,1.16+0,15.30}.100\%\approx26,2\%\\\%m_{C_2H_6}\approx73,8\%\end{matrix}\right.\)
Bạn tham khảo nhé!
56c
57a