Câu 1: Kim loại nào sau đây có thể tan trong dung dịch HNO3 đặc nguội ?
A. Cr. B. Cu. C. Fe. D. Al.
Câu 2: Phát biểu nào sau đây không đúng?
A. Tính dẫn điện của kim loại bạc tốt hơn kim loại đồng. B. Các kim loại kiềm ( nhóm IA) đều có trúc mạng tinh thể lập phương tâm khối.
C. Từ P và HNO3 đặc, nóng có thể điều chế được H3PO4. D. Có thể dùng CO để làm khô khí HCl có lẫn hơi nước.
Câu 3: Cho m gam hỗn hợp X gồm CuO, Fe2O3, FeO tác dụng vừa đủ với 100ml dung dịch chứa H2SO4 1M và HCl 1M. Thể tích (ở đktc) hỗn hợp khí CO và H2 tối thiểu cần dùng để khử hoàn toàn m gam hỗn hợp X là
A. 3,36 lít. B. 6,72 lít. C. 1,12 lít. D. 4,48 lít.
Câu 4: Dung dịch nào sau đây có khả năng làm nhạt màu dung dịch KMnO4 trong môi trường H2SO4 ?
A. Fe2(SO4)2. B. CuSO4. C. FeSO4. D. Fe(NO3)3
Câu 5: Cho các phát biểu sau: (1) Để một miếng gang ( hợp kim sắt – cacbon) ngoài không khí ẩm, sẽ xảy ra ăn mòn điện hóa. (2) Kim loại cứng nhất là W (vonfam). (3) Hòa tan Fe3O4 bằng dung dịch HCl vừa đủ, thu được dung dịch chứa hai muối. (4) Khi điện phân NaCl nóng chảy (điện cực trơ), tại catot xảy ra sự oxi hóa ion Na+. (5) Không thể dùng khí CO2 để dập tắt đám cháy magie hoặc nhôm. Số phát biểu đúng là
A. 4. B. 3. C. 1. D. 2.
Câu 6: Cho m gam bột Fe vào 200 ml dung dịch chứa HCl 0,4M và Cu(NO3)2 0,2M. Lắc đều cho các phản ứng xảy ra hoàn toàn, sau phản ứng thu được hỗn hợp chất rắn có khối lượng bằng 0,75m gam và V lít (ở đktc) khí NO (sản phẩm khử duy nhất của N+5). Giá trị của m và V lần lượt là:
A. 3,84 và 0,448. B. 5,44 và 0,896. C. 5,44 và 0,448. D. 9,13 và 2,24.
Câu 7: Cho 23 gam hỗn hợp X gồm Cu, Fe, Cu2S, CuS, FeS2 và FeS tác dụng hết với dung dịch HNO3 (đặc nóng, dư) thu được V lít (ở đktc) khí NO2 duy nhất và dung dịch Y. Nếu cho toàn bộ Y vào một lượng dư dung dịch BaCl2, thu được 58,25 gam kết tủa. Mặt khác, khi cho toàn bộ Y tác dụng với dung dịch NaOH dư thu được 25,625 gam chất kết tủa. Giá trị của V là
A. 16,8. B. 38,08. C. 24,64. D. 47,6.
Câu 8: Cho 74,88 gam hỗn hợp rắn X gồm Fe, Fe3O4 và Fe(NO3)2 vào dung dịch chứa 0,3 mol HCl và 0,024 mol HNO3, khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Y (không chứa NH4+) và 0,032 mol hỗn hợp khí Z gồm NO và N2O. Cho dung dịch AgNO3 đến dư vào dung dịch Y, sau phản ứng thấy thoát ra 0,009 mol NO (sản phẩm khử duy nhất của N+5), đồng thời thu được 44,022 gam kết tủa. Phần trăm khối lượng Fe trong hỗn hợp X có giá trị gần nhất với giá trị nào sau đây?
A. 46,6%. B. 37,8%. C. 35,8%. D. 49,6%.
Câu 9: Cho các miếng sắt nhỏ vào dung dịch sau: (1) HCl; (2) NaOH; (3) NaNO3; (4) FeCl3. Số trường hợp xảy ra phản ứng hóa học là
A. 4. B. 2. C. 1. D.3.
Câu 10: Các kim loại X, Y và Z đều không tan trong nước ở điều kiện thường X và Y đều tan trong dung dịch HCl nhưng chỉ có Y tan trong dung dịch NaOH. Z không tan trong dung dịch HCl nhưng tan trong dung dịch HNO3 loãng, đun nóng. Các kim loại X, Y và Z tương ứng là A. Fe, Al và Cu. B. Mg, Fe và Ag. C. Na, Al và Ag. D. Mg, Alvà Au.









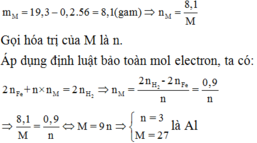

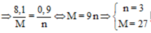
Câu 1 : B
Câu 2 : D
Câu 3 : A
Ta có : \(nO\left(trong.oxit\right)=\frac{1}{2}nH^+\)
mà \(\Sigma nH^+=2.0,1.1+0,1.1=0,3\left(mol\right)\)
=> nO(trong oxit) = 0,15mol => nCO + nH2 = nO = 0,15mol => Vhh = 0,15.22,4 = 3,36(l)
câu 4: C
Câu 5 : A ( gồm 1,2,3 và 5)
Câu 6 : C
Ta có :
H+: 0,08
NO3-: 0,08
3Fe + 8H+ + 2NO3-→3Fe2+ + 2NO + 4H2O
0,03 0,08 0,02
Fe + Cu2+ → Fe2+ + Cu
0,04 0,04 0,04
m chất rắn = m Fe dư + mCu => m - 0,07.56 + 64.0,04 = 0,75m => m = 5,44 gam VNO = 0,02.22,4 = 0,448 lít
Câu 9 : B ( Fe + HCl và Fe + FeCl3 )
Câu 10 : A
Câu 8 :
Phần kết tủa có nAgCl= 0,3 => nAg = 0,009
Bảo toàn electron: nFe2+ = nAg + 3nNO = 0,036
nNO = 0,009 => nH+ dư = 4nNO = 0,036
Đặt a, b, c là số mol Fe, Fe3O4, Fe(NO3)2 trong X => mX = 56a + 232b + 180c = 7,488 (1 )
Dung dịch Y còn H+ dư và Fe2+ nên NO3- đã hết. Vậy Y chứa Fe2+ (0,036), H+ (0,036), Cl- (0,3)
Bảo toàn điện tích => nFe3+ = 0,064
Bảo toàn Fe => a + 3b + c = 0,064 + 0,036 (2)
Bảo toàn H => nH2O = 0,144
Bảo toàn O: 4nFe3O4 + 6nFe(NO3)2 + 3nHNO3 = nZ + nH2O => 4b + 6c + 0,024 . 3 = 0,032 + 0,144 (3)
Giải hệ (1)(2)(3): a = 0,05 b = 0,014 c = 0,008 => %Fe = 37,4%