Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:4P+5O_2\underrightarrow{t^o}2P_2O_5\\ LTL:\dfrac{0,2}{4}< \dfrac{0,4}{5}\Rightarrow O_2dư\)
\(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=\dfrac{5}{4}.0,2=0,25\left(mol\right)\\ n_{O_2\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(n_{P_2O_5\left(lt\right)}=\dfrac{1}{2}n_P=\dfrac{1}{2}.0,2=0,1\left(mol\right)\\ m_{P_2O_5\left(lt\right)}=0,1.142=14,2\left(g\right)\\ m_{P_2O_5\left(tt\right)}=0,1.142.80\%=11,36\left(g\right)\)

a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{4}< \dfrac{0,4}{5}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=0,25\left(mol\right)\Rightarrow n_{O_2\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(\Rightarrow m_{O_2\left(dư\right)}=0,15.32=4,8\left(g\right)\)
c, Theo PT: \(n_{P_2O_5}=\dfrac{1}{2}n_P=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
d, \(m_{P_2O_5}=14,2.80\%=11,36\left(g\right)\)

nP=\(\dfrac{62}{31}\)=0,2(mol)
nO2=\(\dfrac{7,84}{22,4}\)=0,35(mol)
PTHH:4P+5O2to→2P2O5
tpứ: 0,2 0,35
pứ: 0,2 0,25 0,1
spứ: 0 0,1 0,1
a)chất còn dư là oxi
mO2dư=0,1.32=3,2(g)
b)mP2O5=n.M=0,1.142=14,2(g)
\(a.n_P=0,2\left(mol\right);n_{O_2}=0,35\left(mol\right)\\ 4P+5O_2-^{t^o}\rightarrow2P_2O_5\\ LTL:\dfrac{0,2}{4}< \dfrac{0,35}{5}\\ \Rightarrow SauphảnứngO_2dư\\ n_{O_2\left(pứ\right)}=\dfrac{5}{4}n_P=0,25\left(mol\right)\\ \Rightarrow m_{P\left(dư\right)}=\left(0,35-0,25\right).32=3,2\left(g\right)\\ b.n_{P_2O_5}=\dfrac{1}{2}n_P=0,1\left(mol\right)\\ \Rightarrow m_{P_2O_5}=0,1.142=14,2\left(g\right)\)

nP = 2,48/31 = 0,08 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
Mol: 0,08 ---> 0,1 ---> 0,04
mP2O5 = 0,04 . 142 = 5,68 (g)
b) nO2 = 4/32 = 0,125 (mol)
So sánh: 0,125 > 0,1 => O2 dư
nO2 (dư) = 0,125 - 0,1 = 0,025 (mol)
mO2 (dư) = 0,025 . 32 = 0,8 (g)

nP = 6.2/31 = 0.2 (mol)
nO2 = 6.72/22.4 = 0.3 (mol)
4P + 5O2 -to-> 2P2O5
0.2___0.25_____0.1
mO2 dư = ( 0.3 - 0.25) * 32 = 1.6(g)
mP2O5 = 0.1*142 = 14.2 (g)
Ta có: \(n_P=\dfrac{6.2}{31}=0.29mol\)
\(n_{O_2}=\dfrac{6.72}{22.4}=0.3mol\)
PTHH:
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
ta có:
\(\left\{{}\begin{matrix}\dfrac{n_{P\left(bra\right)}}{nP_{\left(pthh\right)}}=\dfrac{0.2}{4}=0.05\\\dfrac{n_{O_2\left(bra\right)}}{n_{O_2}\left(pthh\right)}=\dfrac{0.3}{5}=0.06\end{matrix}\right.\)
=> \(O_2\) dư
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
4 ----------->2
0.2---------->0.1=nP2O5
=>\(m_{P_2O_5}=142.0.1=14.2\left(g\right)\)

4P + 5O2 -----to---> 2P2O5
0,4---0,5-----------> 0,2 (mol)
+ n P = 12,4 / 31 = 0,4 (mol)
+nO2 = 13,44 / 22,4 = 0,6 (mol)
Vì nP/4 = 0,1 < n O2 /5 = 0,12
=> Oxi còn thừa sau phản ứng .
mO2 dư = (0,6 - 0,5 ) . 32 = 3,2 (g)
b. chất tạo thành : P2O5
mP2O5 = 0,2 . ( 2.31 + 16 . 5 ) = 28,4 (g)
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\\
n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\
pthh:4P+5O_2\underrightarrow{t^o}2P_2O_5\\
LTL:\dfrac{0,4}{4}< \dfrac{0,6}{5}\)
=> Oxi dư
\(n_{O_2\left(p\text{ư}\right)}=\dfrac{5}{4}n_P=0,5\left(mol\right)\\
m_{O_2\left(d\right)}=\left(0,6-0,5\right).32=3,2\left(g\right)\\
n_{P_2O_5}=\dfrac{1}{2}n_P=0,2\left(mol\right)\\
m_{P_2O_5}=0,2.142=28,4\left(g\right)\)

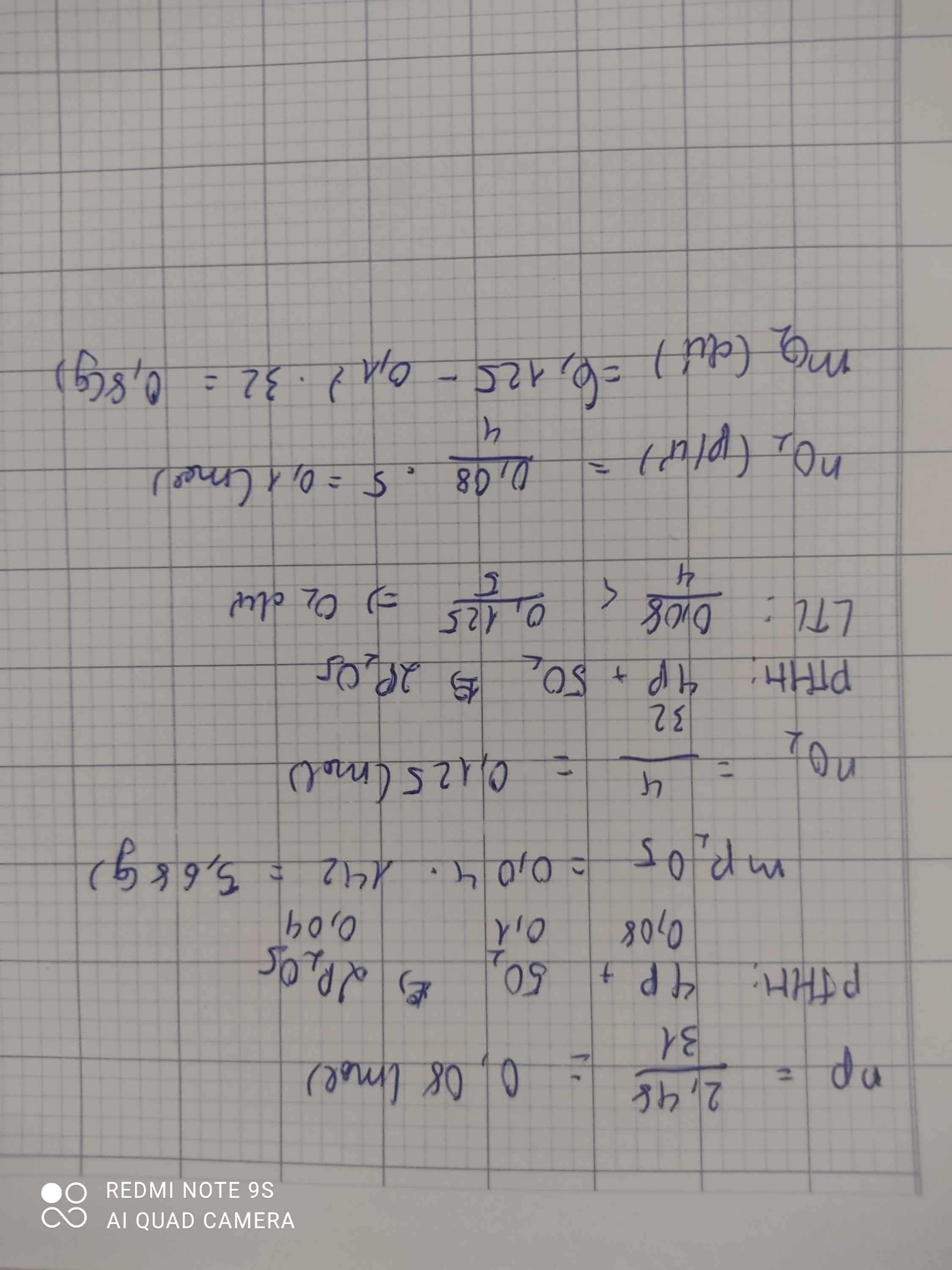
Câu 1. B
Câu 2. D
Câu 3. C
Câu 4. B
Câu 5. C
Câu 6. D
Câu 7. C
Câu 8. D
Câu 9. a) A; b) B
Câu 10. C