Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nồng độ % của dung dịch Na2CO3.
Mdd = V.d = 200 x 1,05 = 210g dung dịch Na2CO3.
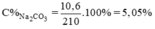
Nồng độ mol/l của dung dịch.
200ml = 0,2l.
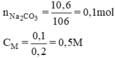

Nồng độ phần trăm của dung dịch pha chế:
- Khối lượng của dung dịch \(Na_2CO_3\):
mdd = \(1,05\cdot200=210\left(g\right)\)
Nòng độ phần trăm của dung dịch:
\(C\%=\frac{100\%\cdot10,6}{210}\approx5,05\%\)
Nồng độ mol của dung dịch pha chế:
- Số mol \(Na_2CO_3\) trong dung dịch:
\(n_{Na_2CO_3}=\frac{10,6}{106}=0,1\left(mol\right)\)
- Nồng độ mol của dung dịch:
\(C_M=\frac{1000\cdot0,1}{200}=0,5\) (mol/ l)

1ml dung dịch cho khối lượng 1,05 gam
200 ml dung dịch cho khối lượng m dd = 210 gam
Nồng độ phần trăm:
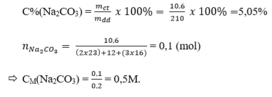

1ml dung dịch cho khối lượng 1,05 gam
200 ml dung dịch cho khối lượng mdd = 210 gam
Nồng độ phần trăm:
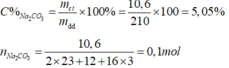
C M Na 2 CO 3 = 0 , 1 : 0 , 2 = 0 , 5 M .

Khối lượng dung dịch Na2CO3:
m = 200 . 1,05 = 210 g
Nồng độ phần trăm của dung dịch:
C% = . 100% = 5,05%
Số mol của Na2CO3 là:
n = = 0,1 mol
Nồng độ mol của dung dịch:
CM = = 0,5 M

\(nNa_2CO_3=\dfrac{10,6}{106}=0,1\left(mol\right)\)
Vdd = 200 ml = 0,2(l)
\(Na_2CO_3+H_2O\rightarrow NaHCO_3+NaOH\)
1 1 1 1 (mol)
0,1 0,1 0,1 0,1 (mol)
theo đề ta suy ra : mdd = 1,05 . 200 = 210 (g)
\(mNaHCO_3=0,1.84=8,4\left(g\right)\)
\(mNaOH=0,1.40=4\left(g\right)\)
=> ndd sau pứ = 0,1 + 0,1 = 0,2 (mol)
m dd vừa đc pha chế = m NaHCO3 + mNaOH
= > mdd vừa đc pha chế = \(8,4+4=12,4\left(g\right)\)
\(C\%dd=\dfrac{12,4.100}{210}=5,9\%\)
\(CM_{dd}=\dfrac{n_{dd}}{V_{dd}}=\dfrac{0,2}{0,2}=1M\)

....(1)20 gam.....(2)80 gam hoặc....(3) 80ml.....(4)100gam......(5)20%.

Khối lượng dung dịch Na2CO3:
\(m_{Na2CO3}\)= 200 . 1,05 = 210 g
Nồng độ phần trăm của dung dịch:
C% = 10,621010,6210 . 100% = 5,05%
Số mol của Na2CO3 là:
\(n_{Na2CO3}\) = \(\frac{10,6}{42+12+48}\)= 0,1 mol
Nồng độ mol của dung dịch:
CM = \(\frac{0,1.1000}{200}\) = 0,5 M
Nồng độ phần trăm của dung dịch pha chế:
Nồng độ mol của dung dịch: